题目内容
5.(1)通过实验,我们测得了石灰水、碳酸饮料、食醋及食盐水的pH,图中箭头方面表示pH逐渐增大,则表示石灰水的是点D,表示食盐水的是点C(填字母).
(2)不同物质的溶液的酸碱性不同,根据下表中PH的情况判断:
| 盐酸 | CuSO4溶液 | NaCl溶液 | 水 | Na2CO3溶液 | NaOH溶液 | |
| PH | <7 | <7 | =7 | =7 | >7 | >7 |
②pH<7的溶液不一定(填“一定”或“不一定”)是酸溶液.
(3)甲酸(HCOOH)是一种有机酸,它的酸性比碳酸强,比盐酸弱,有刺激性气味和较强的腐蚀性.蚂蚁、蚊虫叮咬时会分泌出甲酸,所以甲酸又俗称蚁酸.人被蚊虫叮咬后会痒痛,可以涂抹下列物质中的(填序号)③⑤消除.
①稀盐酸 ②食醋 ③肥皂水 ④食盐水 ⑤稀氨水
(4)白蚂蚁除了会蛀蚀木头外,它分泌的蚁酸还会腐蚀很多建筑材料,下列建筑材料不容易被蚁酸腐蚀的是(填字母)B.
A.镀锌水管 B.铜制塑像 C.大理石栏杆 D.铝合金门窗 E.钢筋.
分析 (1)当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性.食盐水显中性,据此判断.
(2)根据表格中的信息分析溶液的酸碱性,酸溶液显酸性,碱溶液显碱性,盐溶液可能显中性、酸性或碱性,例如碳酸钠溶液属于盐溶液,却显碱性.
(3)人被蚊虫叮咬后会痒痛,是因为蚊虫叮咬时会分泌出甲酸,可以依据中和反应的原理,涂抹显碱性的物质.
(4)根据酸的化学性质进行分析,活泼金属、碳酸盐等都能和酸反应,能和酸反应就容易被酸腐蚀.
解答 解:(1)石灰水呈碱性,pH大于7;碳酸饮料、食醋呈酸性,pH小于7;食盐水呈中性,pH=7,按照溶液pH逐渐增大的顺序,表示石灰水的是点D,表示食盐水的是点C.
(2)①Na2CO3溶液的pH大于7,显碱性,因此加入无色酚酞试液,试液变红色;
②pH<7不一定是酸的溶液,例如CuSO4溶液的pH小于7,但属于盐溶液;
(3)人被蚊虫叮咬后会痒痛,是因为蚊虫叮咬时会分泌出甲酸,可涂抹显碱性的物质.①稀盐酸、②食醋显酸性,不符合要求;④食盐水显中性,不符合要求;③肥皂水显碱性,符号要求;⑤稀氨水显碱性且腐蚀性较小,也可以.
(4)A、锌能与蚁酸发生置换反应,易被腐蚀,故选项错误.
B、铜的金属活动性比氢弱,不能与蚁酸发生化学反应,不易被腐蚀,故选项正确.
C、大理石的主要成分是碳酸钙,能与蚁酸发生复分解反应,易被腐蚀,故选项错误.
D、铝合金的主要成分是铝,能与蚁酸发生置换反应,易被腐蚀,故选项错误.
E、钢筋的主要成分是铁,能与蚁酸发生置换反应,易被腐蚀,故选项错误.
故填:(1)D;C;(2)①红; ②不一定;(3)③⑤;(4)B.
点评 本题难度不大,掌握pH与溶液酸碱性的关系、中和反应应用、酸的化学性质(与活泼金属、金属氧化物、碳酸盐、碱等物质反应)是正确解答本题的关键.

| A. | 干冰易升华 | B. | 浓盐酸易挥发 | C. | 氢气可燃烧 | D. | 酒精易挥发 |
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
(2)反应过程中产生氢气的质量是多少?
(3)最后烧杯中所盛物质的总质量是多少?
| A. | 取液体后的胶头滴管,平放在桌面上 | |
| B. | 用镊子夹取块状药品 | |
| C. | 把块状固体横放在试管口,再慢慢将试管直立起来 | |
| D. | 用胶头滴管滴加液体时,胶头滴管悬空垂直于容器上方 |
| A. | 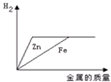 向等质量等浓度的稀盐酸中逐渐加入铁粉和锌粉,产生H2的质量随加入金属的变化关系 | |
| B. | 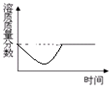 向一饱和澄清石灰水中加入一定量的氧化钙后,所得溶液的溶质质量分数随时间变化关系 | |
| C. | 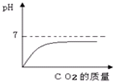 向一定量的水中持续通入二氧化碳气体,所得溶液的pH随通入二氧化碳质量的变化关系 | |
| D. | 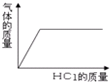 向部分变质的NaOH溶液中逐滴滴加稀盐酸,产生气体随加入稀盐酸质量的变化关 |
| A. | 将气体分别通入蒸馏水中 | B. | 将气体分别通入澄清的石灰水中 | ||
| C. | 将燃着的木条分别伸入集气瓶中 | D. | 以上三种方法都可以 |
