题目内容
15. 铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡,故又称假银箔.小柯用放置很久的铝箔与稀盐酸反应,如图横坐标表示反应时间,根据图象判断,纵坐标可以表示的信息是在0~t1时间段内,氢气的质量为0,原因是:铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,氧化铝与稀盐酸反应没有气泡生成;t1~t2时间段产生氢气的速率快,此时盐酸溶质的质量分数较大,铝和稀盐酸反应剧烈,t2~t3时间段产生氢气速度放缓的原因是稀盐酸的溶质质量分数在反应中逐渐降低.,并作出解答.
铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡,故又称假银箔.小柯用放置很久的铝箔与稀盐酸反应,如图横坐标表示反应时间,根据图象判断,纵坐标可以表示的信息是在0~t1时间段内,氢气的质量为0,原因是:铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,氧化铝与稀盐酸反应没有气泡生成;t1~t2时间段产生氢气的速率快,此时盐酸溶质的质量分数较大,铝和稀盐酸反应剧烈,t2~t3时间段产生氢气速度放缓的原因是稀盐酸的溶质质量分数在反应中逐渐降低.,并作出解答.
分析 根据氧化铝、铝的性质及随着反应的进行溶液的浓度逐渐降低进行分析回答.
解答 解:在0~t1时间段内,氢气的质量为0,原因是:铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,氧化铝与稀盐酸反应没有气泡生成;t1~t2时间段产生氢气的速率快,此时盐酸溶质的质量分数较大,铝和稀盐酸反应剧烈,t2~t3时间段产生氢气速度放缓的原因是稀盐酸的溶质质量分数在反应中逐渐降低.
故答案为:在0~t1时间段内,氢气的质量为0,原因是:铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,氧化铝与稀盐酸反应没有气泡生成;t1~t2时间段产生氢气的速率快,此时盐酸溶质的质量分数较大,铝和稀盐酸反应剧烈,t2~t3时间段产生氢气速度放缓的原因是稀盐酸的溶质质量分数在反应中逐渐降低.
点评 本题考查了铝的化学性质,掌握金属氧化物、金属与酸反应的规律是解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.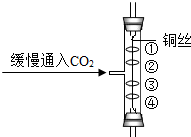 如图所示,管中①④为用紫色石蕊试液润湿的棉球,②③为浸过紫色石蕊试液的干燥棉球,将CO2缓缓通入,则下列描述的实验现象正确的是( )
如图所示,管中①④为用紫色石蕊试液润湿的棉球,②③为浸过紫色石蕊试液的干燥棉球,将CO2缓缓通入,则下列描述的实验现象正确的是( )
 如图所示,管中①④为用紫色石蕊试液润湿的棉球,②③为浸过紫色石蕊试液的干燥棉球,将CO2缓缓通入,则下列描述的实验现象正确的是( )
如图所示,管中①④为用紫色石蕊试液润湿的棉球,②③为浸过紫色石蕊试液的干燥棉球,将CO2缓缓通入,则下列描述的实验现象正确的是( )| A. | ④比①先红,②③不变红 | B. | ①比④先红,②③不变红 | ||
| C. | ④变红,①②③不变红 | D. | ①变红,②③④不变红 |
10.实验是学习科学的重要方法.以下是四位同学通过实验得出的结论,期中正确的是( )
| A. | 在碳酸钠溶液中,滴加无色酚酞试液,溶液变成红色,说明碳酸钠属于可溶性碱 | |
| B. | 在铁和硫反应实验中,磁铁吸起了铁粉,不能吸起加热后的物质,说明铁和硫能反应 | |
| C. | 将氯化钡溶液滴入到某无色溶液中,产生白色沉淀,说明该无色溶液一定含硫酸根 | |
| D. | 将稀盐酸滴入到某固体中,发现有气泡产生,证明该固体是碳酸盐 |
20.工业上通过在石灰窑中煅烧石灰石制得“石灰”,其反应原理是:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.科学兴趣小组的同学对某地刚出窑的“石灰”样品的成分进行探究.
【提出问题】刚出窑的“石灰”样品有哪样成分?
【猜想】Ⅰ:只有氧化钙Ⅱ:只有碳酸钙Ⅲ:既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入定量的水,振荡,有白色不溶物,甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立,乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生,乙同学据此认为试管中的固体只有氧化钙,即猜想Ⅰ成立,丙同学认为猜想Ⅰ不成立,理由是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡;
(3)小组同学讨论后,设计了如下实验方案并证明了猜想Ⅲ成立.
【提出问题】刚出窑的“石灰”样品有哪样成分?
【猜想】Ⅰ:只有氧化钙Ⅱ:只有碳酸钙Ⅲ:既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入定量的水,振荡,有白色不溶物,甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立,乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生,乙同学据此认为试管中的固体只有氧化钙,即猜想Ⅰ成立,丙同学认为猜想Ⅰ不成立,理由是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡;
(3)小组同学讨论后,设计了如下实验方案并证明了猜想Ⅲ成立.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡,过滤取滤液滴加无色酚酞试液 ②取少量固体于试管中,滴加足量的稀盐酸 | 溶液变红 有气泡产生 | 既有氧化钙也有碳酸钙 |
7.下列除去混合物中少量杂质(括号内为杂质)的方法中,不正确的是( )
| 混合物 | 选用物质 |
| A.CO(CO2) | 过量的氢氧化钠溶液 |
| B.CaCl2(HCl) | 过量的碳酸钙 |
| C.HCl(BaCl2) | 过量的硫酸铜溶液 |
| D.FeSO4(CuSO4) | 过量的铁粉 |
| A. | A | B. | B | C. | C | D. | D |
5.某化工厂排放的污水中可能含有氯化钠、硫酸钠、碳酸钠.某科学兴趣小组从污水中取样对其成分进行验证:
(1)若要用pH试纸测定该河水的酸碱度其正确的操作方法用玻璃棒取待测液滴在pH试纸上,所显示的颜色与标准比色卡对照.
(2)要证明污水中是否含有氯化钠、硫酸钠、碳酸钠,写出简单的验证方案如表.
(1)若要用pH试纸测定该河水的酸碱度其正确的操作方法用玻璃棒取待测液滴在pH试纸上,所显示的颜色与标准比色卡对照.
(2)要证明污水中是否含有氯化钠、硫酸钠、碳酸钠,写出简单的验证方案如表.
| 实验步骤 | 实验现象 | 结论 |
| ①取样加入足量 硝酸溶液 | 有气泡 | 含有碳酸钠 |
| ②取步骤1中反应后的溶液加足量的 硝酸钡溶液 | 白色沉淀 | 含有硫酸钠 |
| ③过滤 | ||
| ④在滤液中,滴加硝酸银溶液 | 有白色沉淀 | 含有氯化钠 |
 如图,用细线将一根粗细均匀的硬质铜丝悬挂起来,调节细线位置使之处于铜丝中点,此时铜丝保持水平平衡.
如图,用细线将一根粗细均匀的硬质铜丝悬挂起来,调节细线位置使之处于铜丝中点,此时铜丝保持水平平衡.