题目内容
9.对超市一种新产品…“污渍爆炸盐”有关问题进行探究,该产品的说明书如下:[主要成分]过氧碳酸钠.
[用 途]衣物助洗剂,能在瞬间去除洗衣粉难以除去的多种顽固污渍.
[注意事项]使用时避免接触皮肤
查阅资料得知:过氧碳酸钠(Na2CO4)俗称“固体双氧水”,白色结晶颗粒.“污渍爆炸盐”溶于水后,Na2CO4与H2O反应只生成2种物质,1种是碳酸盐,另1种是化合物.
活动一:检验爆炸盐溶于水后是否生成碳酸钠
| 实验步骤 | 实验现象 | 结论 |
| 取水量爆炸盐溶于水后的溶液于试管中,加入稀盐酸并且将生成的气体通入澄清石灰水 | (1)产生大量气泡,澄清石灰水变浑浊 | 爆炸盐溶于水后的溶液存在碳酸钠 |
(1)猜想假设:猜想一:可能是NaOH
猜想二:可能为H2O2,作出以上猜想的依据是质量守恒定律.
(2)实验探究:
| 实验步骤 | 实验现象 | 结论 |
| 实验一:(1)取少量爆炸盐溶液加入足量的氯化钙溶液 (2)过滤,向滤液中滴加酚酞试液 | (1)产生白色沉淀 (2)酚酞不变色 | 该含氧化合物不是NaOH |
| 实验二:取少量二氧化锰于试管中,滴加适量的爆炸盐溶液,并将带火星的木条伸入其中 | 产生气泡 带火星的木条复燃 | 产生了氧气,该含氧化合物为过氧化氢. |
分析 活动一:
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊;
活动二:
化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类和总个数不变;
碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,氢氧化钠溶液显碱性,能使酚酞试液变红色;
氧气能使带火星的木条复燃;
根据物质的性质可以判断保存方法.
解答 解:活动一:
实验过程如下表所示:
| 实验步骤 | 实验现象 | 结论 |
| 取适量爆炸盐溶于水后的溶液于试管中,加入稀盐酸并且将生成的气体通入澄清石灰水 | (1)产生大量气泡,澄清石灰水变浑浊 | 爆炸盐溶于水后的溶液存在碳酸钠 |
(1)猜想假设:猜想一:可能是NaOH
猜想二:可能为H2O2,作出以上猜想的依据是质量守恒定律.
故填:质量守恒定律.
(2)实验探究如下表所示:
| 实验步骤 | 实验现象 | 结论 |
| 实验一:(1)取少量爆炸盐溶液加入足量的氯化钙溶液 (2)过滤,向滤液中滴加酚酞试液 | (1)产生白色沉淀 (2)酚酞不变色 | 该含氧化合物不是NaOH |
| 实验二:取少量二氧化锰于试管中,滴加适量的爆炸盐溶液,并将带火星的木条伸入其中 | 产生气泡,带火星的木条复燃 | 产生了氧气,该含氧化合物为过氧化氢. |
故填:密封.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
5.在FeO、Fe2O3、Fe3O4三种化合物中,与等质量铁相结合的氧的质量比是( )
| A. | 1:3:4 | B. | 6:9:8 | C. | 6:8:9 | D. | 6:1:4 |
17.潜艇内的氧气再生设备主要为氧气再生药板,“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na2O2),过氧化钠使用后变成白色固体.现对白色固体的成分进行探究:
【查阅资料】2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2↑
【提出猜想】根据人体呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:
猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
【得出结论】猜想Ⅲ成立.
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
【查阅资料】2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2↑
【提出猜想】根据人体呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:
猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入适量氯化钙溶液; | 产生白色沉淀; | 该反应的化学方程式为Na2CO3+CaCl2=2NaCl+CaCO3↓; |
| (2)将上述反应后的混合物过滤,取滤液加入无色酚酞试液. | 无色变红色. | 证明猜想Ⅲ正确 |
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
14.金属M和AgNO3溶液反应的化学方程式为:M+2AgNO3═M(NO3)2+2Ag.则下列说法错误的是( )
| A. | 这个反应属于置换反应 | |
| B. | 金属M可能是铜 | |
| C. | 用M可以回收硝酸银废液中的银 | |
| D. | 反应前后元素M和N化合价发生了变化 |
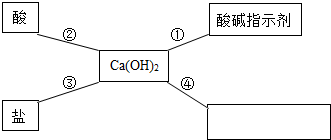 对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应.
对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应. 是某些非金属氧化物.
是某些非金属氧化物.
