题目内容
17.下列实验操作错误的是( )| A. | 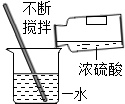 稀释浓硫酸 | B. | 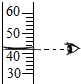 液体的量取 | ||
| C. |  给液体加热 | D. |  往试管里送入固体粉末 |
分析 A、浓硫酸的稀释方法:“酸入水,沿器壁,慢慢倒,不断搅.”
B、读数时,量筒必须放平,视线要跟量筒内液体的凹液面的最低处保持水平,再读出液体体积.
C、使用酒精灯的外焰给试管内的液体加热.
D、取用时可以用药匙(或者纸槽).操作要领是:“一斜、二送、三直立”.
解答 解:A、浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌,操作正确;
B、读数时,视线要跟量筒内液体的凹液面的最低处保持水平,再读出液体体积,操作正确;
C、应该利用酒精灯的外焰给试管内的液体加热,操作错误;
D、粉末状药品的取用方法:先将试管倾斜,把盛药品的药匙(或者纸槽)小心地送入试管底部,再使试管直立起来,操作正确;
故选:C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
5.6g碳单质全部燃烧生成气体,生成气体的总质量不可能( )
| A. | 22g | B. | 20g | C. | 14g | D. | 12g |
2.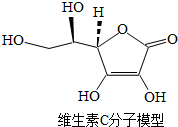 维生素C(化学式为C6H8O6)是人体必须的营养物质,能提高免疫力,预防癌症,保护牙龈等.下列有关维生素C的说法正确的是( )
维生素C(化学式为C6H8O6)是人体必须的营养物质,能提高免疫力,预防癌症,保护牙龈等.下列有关维生素C的说法正确的是( )
 维生素C(化学式为C6H8O6)是人体必须的营养物质,能提高免疫力,预防癌症,保护牙龈等.下列有关维生素C的说法正确的是( )
维生素C(化学式为C6H8O6)是人体必须的营养物质,能提高免疫力,预防癌症,保护牙龈等.下列有关维生素C的说法正确的是( )| A. | 维生素C属于氧化物 | |
| B. | 维生素C中碳、氢、氧元素的质量比为3:4:3 | |
| C. | 维生素C分子中质子数和电子数一定相等 | |
| D. | 维生素C由碳、氢、氧三种原子构成 |
6.某化学兴趣小组同学对碳酸钙高温加热一段时间剩余固体的成分进行探究.

(1)碳酸钙高温下发生分解的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
[探究活动一]剩余固体的成分
(2)同学们按照下表所示的步骤进行实验,请你参与:
[探究活动二]测定剩余固体中碳酸钙的质量分数
方案一:称取剩余固体试样11.0g,利用如图1装置进行实验测定.
数据记录如下:
(3)生成CO2的质量为4.4g.
(4)反应容器中生成CO2的化学方程式为CaCO3+2HCl═CaCl+H2O+CO2↑.
(5)通过计算确定试样中碳酸钙的质量分数大约为90.9%(保留一位小数).
(6)下列情况中,会导致测定结果偏低的是A(填标号)
A、反应容器中有CO2残留 B、HCl气体和水蒸气随CO2气体排出 C、滴入的稀盐酸排出的气体
方案二:另取剩余固体试样,按图2所示的实验步骤进行实验:
(7)步骤②加入的水要足量,其目的是使氧化钙(填“氧化钙”、“碳酸钙”)完全溶解.
(8)不溶物的质量与试样的质量的比值即碳酸钙的质量分数,若测定结果偏大,可能原因是加入的水不足,氧化钙没有完全溶解;(或不溶物碳酸钙没有洗净,或不溶物没有完全干燥)(写一点).

(1)碳酸钙高温下发生分解的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
[探究活动一]剩余固体的成分
(2)同学们按照下表所示的步骤进行实验,请你参与:
| 操作 | 现象 | 解释或结论 |
| ①取少量固体于试管中,加适量水振荡,用手触摸 试管外壁;静置,滴入 几滴无色酚酞试液 | 试管外壁发烫; 酚酞试液变红色. | 说明剩余固体中含有氧化钙.氧化钙 溶于水生成氢氧化钙,同时放出(填“放出”或“吸收”)热量. |
| ②再取少量固体于另一 试管中滴加过量稀盐酸 | 试管中有气泡产生 | 说明剩余固体中含有碳酸钙. |
方案一:称取剩余固体试样11.0g,利用如图1装置进行实验测定.
| 时间 | 称量项目 | 质量/g |
| 反应开始前 | 装置+稀盐酸+试样 | 171.0 |
| 反应结束后 | 装置+稀盐酸+试样 | 166.6 |
(3)生成CO2的质量为4.4g.
(4)反应容器中生成CO2的化学方程式为CaCO3+2HCl═CaCl+H2O+CO2↑.
(5)通过计算确定试样中碳酸钙的质量分数大约为90.9%(保留一位小数).
(6)下列情况中,会导致测定结果偏低的是A(填标号)
A、反应容器中有CO2残留 B、HCl气体和水蒸气随CO2气体排出 C、滴入的稀盐酸排出的气体
方案二:另取剩余固体试样,按图2所示的实验步骤进行实验:
(7)步骤②加入的水要足量,其目的是使氧化钙(填“氧化钙”、“碳酸钙”)完全溶解.
(8)不溶物的质量与试样的质量的比值即碳酸钙的质量分数,若测定结果偏大,可能原因是加入的水不足,氧化钙没有完全溶解;(或不溶物碳酸钙没有洗净,或不溶物没有完全干燥)(写一点).


 “人工智能”正逐步进入汽车制造领域,无人驾驶主要依靠车内的智能驾驶系统来实现.
“人工智能”正逐步进入汽车制造领域,无人驾驶主要依靠车内的智能驾驶系统来实现. A~D是初中化学常见的物质,其中A为黑色固体,D为蓝色沉淀,它们之间的相互转化 关系如图所示,其中部分生成物和反应条件已省略.
A~D是初中化学常见的物质,其中A为黑色固体,D为蓝色沉淀,它们之间的相互转化 关系如图所示,其中部分生成物和反应条件已省略.