题目内容
5.6g碳单质全部燃烧生成气体,生成气体的总质量不可能( )| A. | 22g | B. | 20g | C. | 14g | D. | 12g |
分析 因为已知碳在氧气中充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,而此题最终生成的气体可能是二氧化碳,也可能是一氧化碳,也可能是二者的混合物.所以首先假设6g碳在氧气中完全燃烧,计算出所得二氧化碳的质量;然后假设6碳在氧气中不完全燃烧,计算出所得一氧化碳的质量,那么最终气体的质量就在这两个数值之间.
解答 解:设6g碳在氧气中完全燃烧生成二氧化碳的质量为x
C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
12 44
6g x
$\frac{12}{44}=\frac{6g}{x}$ 解得:x=22g
再假设6g碳在氧气中不充分燃烧产生的一氧化碳的质量为y
2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO
24 56
6g y
$\frac{24}{56}=\frac{6g}{y}$ 解得:y=14g
碳和氧气完全反应生成的气体的质量应该≥14g,而≤22g.所以D不正确
故选D.
点评 此题考查的是利用化学方程式的计算,此题中因为碳和氧气反应的方程式有两个,所以要判断最后所得气体的质量一般用的方法就是极端假设法,同学们只要掌握了这个方法就可以解决这一类的问题.

练习册系列答案
相关题目
20.下列关于对化学实验操作的描述中正确的是( )
| A. | 给试管中的液体加热,液体不能超过试管容积的$\frac{1}{2}$ | |
| B. | 加热过的试管,不能立即用冷水冲洗 | |
| C. | 向盛有一定量浓硫酸的试管中,滴加蒸馏水进行稀释 | |
| D. | 用嘴小心吹灭燃着的酒精灯 |
17.下列实验操作错误的是( )
| A. | 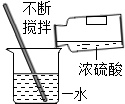 稀释浓硫酸 | B. | 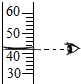 液体的量取 | ||
| C. |  给液体加热 | D. |  往试管里送入固体粉末 |