题目内容
1.近年来,我市积极探索建设社会主义新农村的服务体系,许多农户获得“测土配方施肥”服务,有效解决了施肥比例不合理问题,提高了产量,减少了环境污染.小明家种了一片麦子,经农科人员测定该片土壤需补充钾元素39千克.(1)请你帮小明算算,至少需购买氯化钾(KCl)多少千克?
(2)小明家原来准备用硝酸铵(NH4NO3),农科人员告诉他们需要120千克,但市场上硝酸铵缺货,只有尿素,问:需要购买多少千克的尿素[CO(NH2)2]才与120千克硝酸铵有相同的氮元素?
分析 (1)根据氯化钾(KCl)中钾元素的质量,进行分析解答;
(2)结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)设至少需购买氯化钾(KCl)xkg,则
$\frac{39}{39+35.5}$×100%x=39kg x=74.5kg.
(2)120kg硝酸铵中含氮质量=120kg×$\frac{14×2}{14×2+1×4+16×3}$×100%=42kg,
含42kg氮元素的尿素质量=42kg÷$\frac{14×2}{12+16+14×2+1×4}$×100%=90kg.
答:(1)至少需购买氯化钾(KCl)74.5千克;
(2)需要购买90千克的尿素[CO(NH2)2]才与120千克硝酸铵有相同的氮元素.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
3.除去下列物质中的少量杂质,所用试剂或方法错误的是( )
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | 二氧化锰 | 泥沙 | 加水溶解,过滤 |
| B | 氯化钠 | 碳酸钠 | 加入过量稀盐酸,加热蒸发 |
| C | 二氧化碳 | 一氧化碳 | 将气体通过灼热的氧化铜 |
| D | 氯化钙溶液 | 稀盐酸 | 加入过量碳酸钙,过滤 |
| A. | A | B. | B | C. | C | D. | D |
4.本学期,学校开展了“五水共治”手抄报比赛,同学们都认识到了水资源的重要性.下列有关地球上水的说法错误的是( )
| A. | 从冰箱里取出一瓶饮料,一段时间后饮料瓶外壁上出现水珠,这是由于水蒸气遇冷液化形成的.说明了空气中也有水. | |
| B. | 水是生命之源,动植物都离不开水,所以保护水资源是每个公民应尽的义务 | |
| C. | 理论上电解水得到的氢气与氧气的体积比为2:1 | |
| D. | 以上说法都不对 |
9.人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.
(1)金属大规模被使用的先后顺序跟③(填序号)关系最大.
①地壳中金属元素的含量②金属的导电性③金属的活动性
(2)为探究锰与铁的金属的活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中(反应中Mn显+2价).请回答:
除了比较与酸反应产生气体速率的快慢,请你再举出一种可比较这两种金属活动性强弱的方法(写出所需花药品即可):锰和硫酸亚铁溶液;
(3)将一定量的铝加入到硫酸亚铁和硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸,有气泡产生,则滤渣中一定有的物质是Cu、Fe(填化学式).
(4)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是铁.
②若天平失去平衡,则指针一定偏向放铁的一边.
(1)金属大规模被使用的先后顺序跟③(填序号)关系最大.
①地壳中金属元素的含量②金属的导电性③金属的活动性
(2)为探究锰与铁的金属的活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中(反应中Mn显+2价).请回答:
| 金属 | 铁 | 锰 |
| 与盐酸反应的现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |
| 结论 | 活动性铁<(填“>”或“<”)锰 | |
(3)将一定量的铝加入到硫酸亚铁和硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸,有气泡产生,则滤渣中一定有的物质是Cu、Fe(填化学式).
(4)将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
①若天平仍保持平衡,烧杯中一定没有剩余的物质是铁.
②若天平失去平衡,则指针一定偏向放铁的一边.
16. 铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
实验设计:相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等浓度且足量的稀盐酸中反应,观察现象.请分析回答下列问题:
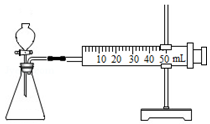
(1)连接仪器组装成如图所示.某学生用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,你认为该装置是否漏气?否.
(2)实验前,用砂纸将两种金属薄片表面擦光亮,其目的是除去金属表面的氧化物.
(3)根据下表中的现象填写结论.
 铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:实验设计:相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等浓度且足量的稀盐酸中反应,观察现象.请分析回答下列问题:
(1)连接仪器组装成如图所示.某学生用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,你认为该装置是否漏气?否.
(2)实验前,用砂纸将两种金属薄片表面擦光亮,其目的是除去金属表面的氧化物.
(3)根据下表中的现象填写结论.
| 金属 | 铁 | 铅 |
| 与盐酸反应现象 | 放出气泡速度较快 | 放出气泡速度较缓慢 |
| 结论 | 铁比铅活泼 | |
11.用浓盐酸配制一定溶质质量分数的稀盐酸,实验时必不可少的一组仪器是( )
| A. | 玻璃棒、量筒、烧杯、胶头滴管 | B. | 托盘天平、玻璃棒、药匙、烧杯 | ||
| C. | 托盘天平、玻璃棒、量筒、烧杯 | D. | 玻璃棒、量筒、烧杯、漏斗 |
 小明和同学用H2O2溶液制取氧气时,错将KMnO4固体当成MnO2放入了H2O2溶液中,结果也发现溶液中迅速产生气泡.小明想:放出的气体是氧气吗?KMnO4固体是H2O2分解的催化剂吗?
小明和同学用H2O2溶液制取氧气时,错将KMnO4固体当成MnO2放入了H2O2溶液中,结果也发现溶液中迅速产生气泡.小明想:放出的气体是氧气吗?KMnO4固体是H2O2分解的催化剂吗? 某科学兴趣小组同学利用如图所示的装置进行实验,当打开止水夹a时,可观察到B试管中的现象是产生气泡;再夹紧止水夹a,可观察到B试管中的现象是产生白色沉淀.
某科学兴趣小组同学利用如图所示的装置进行实验,当打开止水夹a时,可观察到B试管中的现象是产生气泡;再夹紧止水夹a,可观察到B试管中的现象是产生白色沉淀.