题目内容
16.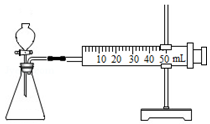 铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:实验设计:相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等浓度且足量的稀盐酸中反应,观察现象.请分析回答下列问题:
(1)连接仪器组装成如图所示.某学生用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,你认为该装置是否漏气?否.
(2)实验前,用砂纸将两种金属薄片表面擦光亮,其目的是除去金属表面的氧化物.
(3)根据下表中的现象填写结论.
| 金属 | 铁 | 铅 |
| 与盐酸反应现象 | 放出气泡速度较快 | 放出气泡速度较缓慢 |
| 结论 | 铁比铅活泼 | |
分析 (1)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(2)实验前,用砂纸将两种金属薄片表面擦光亮,其目的是除去金属表面的氧化物;
(3)金属越活泼,和酸反应速率越快.
解答 解:(1)连接仪器组装成如图所示.某学生用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,说明装置不漏气.
故填:否.
(2)实验前,用砂纸将两种金属薄片表面擦光亮,其目的是除去金属表面的氧化物.
故填:除去金属表面的氧化物.
(3)实验过程如下表所示:
| 金属 | 铁 | 铅 |
| 与盐酸反应现象 | 放出气泡速度较快 | 放出气泡速度较缓慢 |
| 结论 | 铁比铅活泼 | |
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
18.下列物质能发生中和反应并产生沉淀的是( )
| A. | 硫酸和氢氧化钡 | B. | 盐酸和生石灰 | ||
| C. | 碳酸钠和氢氧化钡 | D. | 盐酸和硝酸银 |
19.现用质量分数为 98%的浓硫酸(密度是 1.84g•cm-3)配制 560g 质量分数为 14%的稀硫酸时,下列有关叙述正确的是( )
| A. | 配制稀硫酸时,用到的玻璃仪器只需量筒和烧杯 | |
| B. | 配制稀硫酸时,一定不能用天平称量所需浓硫酸的质量 | |
| C. | 将 480 mL 水倾倒入盛有 80 mL 98%浓硫酸的 500 mL 量筒中 | |
| D. | 将 80 g 98%的浓硫酸沿 1 000 mL 烧杯内壁缓缓倒入 480 mL 水中,并不断搅拌 |
4.通过一年的化学学习,我们已经了解了常见金属在溶液中的活动性顺序,铬(Cr)是重要的金属材料,越来越受到人们的关注,某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
【提出假设】(1)对三种金属的活动性顺序提出的三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.Al>Cu>Cr.
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到体积等浓度的足量稀盐酸中,观察现象,记录如下:
【控制实验条件】
(2)打磨三种金属发生的是物理变化;上述实验使用等浓度的盐酸溶液的理由是盐酸的浓度能够影响反应速率.
【得出结论】
(3)原假设中正确的是a(填假设中a,b或c).写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式Cr+2HCl═CrCl2+H2↑.
【提出假设】(1)对三种金属的活动性顺序提出的三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.Al>Cu>Cr.
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到体积等浓度的足量稀盐酸中,观察现象,记录如下:
| 金属 | Cr | Al | Cu |
| 与盐酸反应发生现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
(2)打磨三种金属发生的是物理变化;上述实验使用等浓度的盐酸溶液的理由是盐酸的浓度能够影响反应速率.
【得出结论】
(3)原假设中正确的是a(填假设中a,b或c).写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式Cr+2HCl═CrCl2+H2↑.
8.继黄金、白金之后,钯金(Pd)首饰在市场上悄然兴起,为了获得钯金,取17.7%的PdCl2溶液100g,加入10.0g铁粉使其充分反应得到钯金和铁的氧化物,经分析所得钯金的质量为10.6g.未反应的铁粉质量为4.4g,下列说法正确的是( )
| A. | 生成铁的氯化物质量为12.7g | B. | 生成铁的氯化物质量为16.25g | ||
| C. | 生成铁的氯化物为FeCl2和FeCl3 | D. | 生成铁的氯化物为FeCl3 |
6.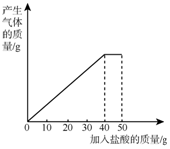 石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
请计算:
(1)由图象可知,第四次加入10g盐酸后,碳酸钙固体又反应掉4克.
(2)完全反应后产生的二氧化碳.
(3)所加盐酸的溶质质量分数.
 石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 16 | 12 | 8 |
(1)由图象可知,第四次加入10g盐酸后,碳酸钙固体又反应掉4克.
(2)完全反应后产生的二氧化碳.
(3)所加盐酸的溶质质量分数.
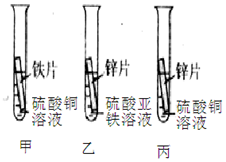 小晨和化学兴趣小组的同学为探究铁、铜、锌的金属活动性顺序,设计了如图三个实验(其中金属均已打磨、其形状、大小及溶液的用量均相同).
小晨和化学兴趣小组的同学为探究铁、铜、锌的金属活动性顺序,设计了如图三个实验(其中金属均已打磨、其形状、大小及溶液的用量均相同).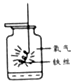 如图为铁丝在氧气中燃烧的实验,回答下列问题:
如图为铁丝在氧气中燃烧的实验,回答下列问题: