题目内容
1.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水,某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究:【提出问题】生成物中有哪种碳的氧化物?
【猜测】
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有二氧化碳 | 含有CO和CO2 |
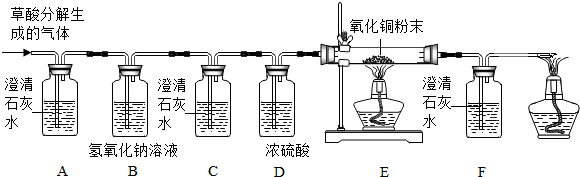
(1)观察到A装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;②E装置中出现黑色粉末变成红色的现象;
【实验结论】通过实验探究证明:猜想3成立.草酸分解的化学方程式是H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+H2O.
【问题讨论】
(1)B装置的作用是除去气体中的二氧化碳,避免对气体中一氧化碳的检验造成干扰;D装置的作用是除去混合气中的水蒸气.
(2)装置末端酒精灯的作用是点燃尾气中一氧化碳,防止污染空气.
分析 【猜想】根据猜想1和3进行分析;
【设计实验】(1)A装置中的澄清石灰水变浑浊,能够证明有CO2气体;
(2)根据一氧化碳有还原性,能和氧化铜反应生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊进行分析;
【实验结论】根据猜想3成立可知,反应物、反应条件、生成物然后写出化学反应式即可;
【问题讨论】
(1)根据氢氧化钠溶液可以吸收二氧化碳气体,浓硫酸有吸水性进行分析;
(2)根据装置末端酒精灯可以处理尾气CO进行分析.
解答 解:【猜想】根据猜想1和3可知,猜想2是只有CO2;
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有二氧化碳 | 含有CO和CO2 |
(2)一氧化碳有还原性,能和氧化铜反应生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊,D装置中黑色粉末变成红色;
【实验结论】根据猜想3成立可知,生成物中有一氧化碳、二氧化碳、水,所以化学反应式是:H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+H2O;
【问题讨论】
(1)澄清石灰水可以检验二氧化碳气体的存在,所以C装置的作用是检验二氧化碳是否被完全吸收;浓硫酸可以吸收水分,所以D装置的作用是吸收水分;
(2)为防止一氧化碳污染空气,装置末端酒精灯可以点燃尾气CO.
故答案为:【猜 想】只有二氧化碳;
【观察分析】(1)A;
(2)①澄清石灰水变浑浊,黑色粉末变成红色;
【实验结论】H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+H2O;
【问题讨论】
(1)除去气体中的二氧化碳,避免对气体中一氧化碳的检验造成干扰,除去混合气中的水蒸气;
(2)点燃尾气中一氧化碳,防止污染空气.
点评 本题是检验一氧化碳和二氧化碳的存在,就要我们熟悉一氧化碳和二氧化碳的性质特点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列关于氯元素符号的书写正确的是( )
| A. | Cl | B. | cL | C. | AL | D. | al |
12.除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是( )
| 物质 | 除杂质选用的试剂 | 操作方法 | |
| A | KCl固体(KClO3) | MnO2,H2O | 加热后加水溶解过滤、蒸发结晶 |
| B | H2(HCl) | Na2CO3溶液、浓H2SO4 | 吸收、干燥 |
| C | KNO3固体(KOH) | H2O、CuSO4溶液 | 溶解、过滤、蒸发结晶 |
| D | CaCl2溶液(HCl) | 过量的CaO | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.小明实验后,把稀硫酸、氢氧化钠溶液和碳酸钠溶液混合一起,看到出现大量气泡.他对反应后溶液中溶质的成分很好奇,请你与他一起进行探究.
【提出问题】反应后溶液中溶质除了含有Na2SO4,还有什么成分?
【猜想假设】猜想①Na2CO3 猜想②Na2CO3、NaOH
猜想③H2SO4 猜想④H2SO4、NaOH
猜想⑤NaOH
小明认为猜想④不合理,理由是硫酸与氢氧化钠能发生中和反应.
【实验探究】(1)取少量该溶液于试管中,向其中滴加无色酚酞,发现溶液变红,据此,可得出的结论是猜想③不成立.
(2)为确定溶液中溶质成分,小明设计下列实验,请你完成下列空白处:
(3)碱溶液使酚酞试液变红,是因为碱在水中解离出OH-(填离子符号,下同),那么属于盐的Na2CO3溶液能使酚酞试液变红,你认为是碳酸钠在水中解离出OH-的缘故.其实Na2CO3溶液能使酚酞试液变红也是由于溶液存在OH-,你认为Na2CO3溶液中存在OH-的原因是CO32-与H2O发生反应产生了OH-.
【提出问题】反应后溶液中溶质除了含有Na2SO4,还有什么成分?
【猜想假设】猜想①Na2CO3 猜想②Na2CO3、NaOH
猜想③H2SO4 猜想④H2SO4、NaOH
猜想⑤NaOH
小明认为猜想④不合理,理由是硫酸与氢氧化钠能发生中和反应.
【实验探究】(1)取少量该溶液于试管中,向其中滴加无色酚酞,发现溶液变红,据此,可得出的结论是猜想③不成立.
(2)为确定溶液中溶质成分,小明设计下列实验,请你完成下列空白处:
| 实验操作 | 实验现象 | 得出的结论 |
| 向步骤(1)的溶液中滴加过量的 稀盐酸溶液 | 开始没有明显变化,后来有气泡产生,最后溶液变成无色 | 猜想②成立,写出该反应的化学方程式: NaOH+HCl=NaCl+H2O;Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
4.6.50g Zn和一定量氯化亚铁溶液,充分反应剩余固体质量为6.05g,若将剩余固体加入到足量稀盐酸中,产生氢气的质量为( )
| A. | 0.20g | B. | 0.22g | C. | 0.18g | D. | 0.21g |