题目内容
7.人体中化学元素含量的多少直接影响健康,缺乏下列哪种元素易导致侏儒症( )| A. | 钙 | B. | 碘 | C. | 锌 | D. | 铁 |
分析 A、根据钙的生理功能和缺乏症进行分析判断.
B、根据碘的生理功能和缺乏症进行分析判断.
C、根据锌的生理功能和缺乏症进行分析判断.
D、根据铁的生理功能和缺乏症进行分析判断.
解答 解:A、钙主要存在于骨胳和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏幼儿和青少年会患佝偻病,老年人会患骨质疏松,故选项错误.
B、碘是合成甲状腺激素的主要元素,缺乏会患甲状腺肿大,故选项错误.
C、锌影响人体发育,缺锌会引起食欲不振,生长迟缓,发育不良,易患侏儒症,故选项正确.
D、铁是合成血红蛋白的主要元素,缺乏会患贫血,故选项错误.
故选:C.
点评 化学元素与人体健康的关系是中考考查的热点之一,熟记人体化学元素的分类、生理功能、缺乏症等是正确解答此类题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列为我区某有机农场栽培的四种有机蔬果的pH,其中呈碱性的是( )
| A. |  柿子pH=8.5 | B. |  西兰花pH=5.6 | C. |  草莓pH=3.2 | D. |  葡萄pH=2.5 |
2.下列各组微粒中,各微粒具有相同电子数的一组是( )
| A. | Na、Mg2+、Al3+ | B. | HF、OH -、NH4+ | C. | S、Cl-、Ar | D. | CH4、NH3、H2S |
12.下列各组离子在pH=2溶液中一定能大量共存的是( )
| A. | Na+ Cl- OH- | B. | Ag+ Cl- NO3- | ||
| C. | Mg2+ Cl- SO42- | D. | K+ Ca2+ CO32- |
19.在一定条件下,木炭、一氧化碳、氢气都能与氧化铜发生反应,下列对这三个反应的分析,正确的是( )
| A. | 所发生的反应都是置换反应 | |
| B. | 反应后都能生成二氧化碳气体 | |
| C. | 反应后都能生成红色的固体 | |
| D. | 反应前后各元素的化合价都发生了变化 |
16.纯碱是重要的化工原料.
制备探究:如图是工业生产纯碱的主要流程示意图.

【查阅资料】
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解.
(1)写出除去粗盐水中MgCl2的化学方程式:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是使溶液显碱性,更多的吸收二氧化碳,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl.
(3)煅烧制得纯碱的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
(4)某海洋化工集团生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,在把100g稀盐酸平均分成四份依次放入样品中,每次均充分反应,实验数据记录如下:
请你据此分析计算:
①第一次加入盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(写出计算过程,结果精确到0.1%)
制备探究:如图是工业生产纯碱的主要流程示意图.

【查阅资料】
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解.
(1)写出除去粗盐水中MgCl2的化学方程式:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是使溶液显碱性,更多的吸收二氧化碳,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl.
(3)煅烧制得纯碱的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
(4)某海洋化工集团生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,在把100g稀盐酸平均分成四份依次放入样品中,每次均充分反应,实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量/g | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(写出计算过程,结果精确到0.1%)
17.现有铜与另一种金属的混合粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.取该混合物粉末8.0g放入烧杯中,将140.0g14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体数据记录如下:
请回答下列问题:
(1)该混合物中铜的质量分数为52.5%;
(2)写出发生反应的化学方程式Mg+H2SO4=MgSO4+H2↑;
(3)根据金属的质量列出第二次加入硫酸后生成气体总质量(x)的比例式$\frac{24}{2.4g}$=$\frac{2}{x}$;
(4)若将第三次反应后溶液蒸发掉8.3g水,则所得不饱和溶液中溶质的质量分数为18%;
(5)如果用98%的浓硫酸配制140.0g的上述所用稀硫酸,则需浓硫酸的质量为20g.
| 次 数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.0 | 35.0 | 35.0 | 35.0 |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
(1)该混合物中铜的质量分数为52.5%;
(2)写出发生反应的化学方程式Mg+H2SO4=MgSO4+H2↑;
(3)根据金属的质量列出第二次加入硫酸后生成气体总质量(x)的比例式$\frac{24}{2.4g}$=$\frac{2}{x}$;
(4)若将第三次反应后溶液蒸发掉8.3g水,则所得不饱和溶液中溶质的质量分数为18%;
(5)如果用98%的浓硫酸配制140.0g的上述所用稀硫酸,则需浓硫酸的质量为20g.
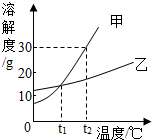 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.