��Ŀ����
16����������Ҫ�Ļ���ԭ�ϣ��Ʊ�̽������ͼ�ǹ�ҵ�����������Ҫ����ʾ��ͼ��

���������ϡ�
�ٴ���ˮ�к�������MgCl2��CaCl2��
�ڳ����£�NH3��������ˮ��CO2������ˮ��
��NaHCO3�����ֽ⣬Na2CO3���Ȳ��ֽ⣮
��1��д����ȥ����ˮ��MgCl2�Ļ�ѧ����ʽ��MgCl2+2NaOH�TMg��OH��2��+2NaCl��
��2���ڹ�ҵ��������������У��ȡ���������̼�ữ����Ŀ����ʹ��Һ�Լ��ԣ���������ն�����̼����̼�ữ��ʱ��NaCl��NH3��CO2����H2O���������NaHCO3��д���÷�Ӧ�Ļ�ѧ����ʽNaCl+NH3+CO2+H2O=NaHCO3+NH4Cl��
��3�������Ƶô���Ļ�ѧ����ʽ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
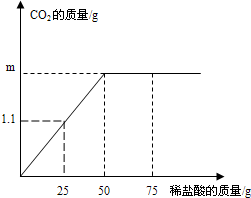
��4��ij�������������Ĵ����Ʒ�к��������Ȼ������ʣ����Ʒ��װ����ע����̼���ơ�96%��Ϊ�ⶨ�ò�Ʒ�к�̼���Ƶ���������������������ʵ�飺ȡ11.0g������Ʒ�����ձ��У��Ƶ��ձ�����ʢ������Ʒ��������Ϊ158.0g���ڰ�100gϡ����ƽ���ֳ��ķ����η�����Ʒ�У�ÿ�ξ���ַ�Ӧ��ʵ�����ݼ�¼���£�
| ��������Ĵ��� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| ���������/g | 25 | 25 | 25 | 25 |
| �ձ�����ʢ����������/g | 181.2 | 204.4 | 228.6 | 253.6 |
�ٵ�һ�μ��������ַ�Ӧ�����ɶ�����̼��������1.8g��
�ڸò�Ʒ��̼���Ƶ����������Ƿ�ϸ�д��������̣������ȷ��0.1%��
���� ��1��Ӧ�����������Ƴ�ȥ�Ȼ�þ���������ƺ��Ȼ�þ��Ӧ����������þ�������Ȼ��ƣ�
��2����������ˮ���ܺ�ˮ��Ӧ���ɰ�ˮ����ˮ�Լ��ԣ�
�Ȼ��ơ�������������̼��ˮ��Ӧ����̼�����ƺ��Ȼ�泥�
��3��̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼��
��4��̼���ƺ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��
��Ӧǰ��������Ϊ��Ӧ���ɶ�����̼�����������ݶ�����̼���������Լ���̼���Ƶ���������һ�����Լ���̼���Ƶ�����������
��� �⣺��1���Ȼ�þ���������Ʒ�Ӧ�Ļ�ѧ����ʽΪ��MgCl2+2NaOH�TMg��OH��2��+2NaCl��
���MgCl2+2NaOH�TMg��OH��2��+2NaCl��
��2���ڹ�ҵ��������������У��ȡ���������̼�ữ����Ŀ����ʹ��Һ�Լ��ԣ���������ն�����̼��
�Ȼ��ơ�������������̼��ˮ��Ӧ����̼�����ƺ��Ȼ�淋Ļ�ѧ����ʽΪ��NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl��
���NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl��
��3��̼���������ȷֽ�Ļ�ѧ����ʽΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
���2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
��4���ٵ�һ�μ��������ַ�Ӧ�����ɶ�����̼������Ϊ��158.0g+25g-181.2g=1.8g��
���1.8��
�����Ʒ��̼���Ƶ�����Ϊx��
̼���ƺ�ϡ���ᷴӦ���ɶ�����̼��������Ϊ��158.0g+100g-253.6g=4.4g��
Na2CO3+2HCl�T2NaCl+H2O+CO2����
106 44
x 4.4g
$\frac{106}{x}$=$\frac{44}{4.4g}$��
x=10.6g��
�ò�Ʒ��̼���Ƶ���������Ϊ��$\frac{10.6g}{11.0g}$��100%=96.4%��
��Ϊ96.4%��96%����˸ò�Ʒ��̼���Ƶ����������ϸ�
���� ��Ϊ̼���ƺ�ϡ���ᷴӦֻ����һ�����������̼����˷�Ӧǰ��������Ϊ��Ӧ���ɶ�����̼��������Ҫע�����⣮

 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�| A�� | ���������ŵ����㣬˵�������ڲ��ϵ��˶� | |
| B�� | ʳ�üӵ��Σ���Ԥ����״���״� | |
| C�� | ��ơ��ƿ�ǣ�ơ�ƻ��Զ����������Ϊ���¶Ȳ���ʱѹǿ��С�������ܽ��Ҳ��С | |
| D�� | ���������У�����к�̼���ߣ�����Ӧ�ù㷺���������ߺ�ҽ������ |
| A�� | �� | B�� | �� | C�� | п | D�� | �� |
| A�� | ����Һ�ж������������ | B�� | ����ҺpH��7 | ||
| C�� | ����Һ�������Ӷ���H+ | D�� | ����Һ����ʹ��ɫʯ����Һ��� |
| A�� |  | B�� |  | ||
| C�� | 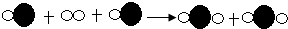 | D�� | 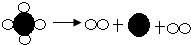 |
| A�� | SO3��H2SO4 | B�� | Ca��OH��2��NaOH | C�� | CuO��Cu��OH��2 | D�� | CaCl2��CaCO3 |
 ������Τ�Ȼ���ע��Һ������H7N9���������е���Чҩ��֮һ��������Τ�Ļ�ѧʽ��C15H28NxO4����
������Τ�Ȼ���ע��Һ������H7N9���������е���Чҩ��֮һ��������Τ�Ļ�ѧʽ��C15H28NxO4����