题目内容
12.写出下列反应的文字表达式:(1)氧化汞受热分解:氧化汞$\stackrel{加热}{→}$汞+氧气
(2)固体液体混合制取氧气:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气
(3)蜡烛在空气中燃烧:蜡烛+氧气$\stackrel{点燃}{→}$水+二氧化碳
(4)实验室用纯净物制氧气:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气
(5)硫燃烧:硫+氧气$\stackrel{点燃}{→}$二氧化硫
其中属于化合反应的是(填序号下同)5,属于分解反应的是1、2、4两者都不是的是3.
分析 (1)根据氧化汞在加热的条件下生成汞和氧气进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
(3)根据蜡烛和氧气在点燃的条件下生成水和二氧化碳进行分析;
(4)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(5)根据硫和氧气在点燃的条件下生成二氧化硫进行分析.
解答 解:(1)氧化汞在加热的条件下生成汞和氧气,文字表达式为:氧化汞$\stackrel{加热}{→}$汞+氧气;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(3)蜡烛和氧气在点燃的条件下生成水和二氧化碳,文字表达式为:蜡烛+氧气$\stackrel{点燃}{→}$水+二氧化碳;
(4)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(5)硫和氧气在点燃的条件下生成二氧化硫,文字表达式为:硫+氧气$\stackrel{点燃}{→}$二氧化硫.
其中属于化合反应的是5,属于分解反应的是1、2、4,两者都不是的是3.
故答案为:(1)氧化汞$\stackrel{加热}{→}$汞+氧气;
(2)过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(3)蜡烛+氧气$\stackrel{点燃}{→}$水+二氧化碳;
(4)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(5)硫+氧气$\stackrel{点燃}{→}$二氧化硫.
5,1、2、4,3.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
2.为弄清实验室里一瓶久置的熟石灰是否部分变质,小明进行了实验探究.请帮小明同学完成实验探究报告.
【提出问题】熟石灰样品是否部分变质?
【猜 想】熟石灰样品已部分变质.其依据是CO2+Ca(OH)2═CaCO3↓十H2O (用化学方程式表示):
【实验仪器与药品】胶头滴管、试管、熟石灰样品、水、酚酞试液、稀盐酸.
【探究过程】
【探究结论】小明的猜想不正确 (填“正确”或“不正确”).
【提出问题】熟石灰样品是否部分变质?
【猜 想】熟石灰样品已部分变质.其依据是CO2+Ca(OH)2═CaCO3↓十H2O (用化学方程式表示):
【实验仪器与药品】胶头滴管、试管、熟石灰样品、水、酚酞试液、稀盐酸.
【探究过程】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量样品加入试管中,加适量的水,振荡,然后滴加酚酞试液 | 溶液变红色 | 样品中存在Ca(OH)2 |
| ②另取少量样品加入另一试管中,然后滴加HCl(或盐酸). | 无气泡产生 | 样品中不存在CaCO3 |
20.某同学用托盘天平称取8.5克某固体药品,称取过程中发现指针向右偏,则他应该( )
| A. | 增加砝码 | B. | 增加药品 | C. | 减少砝码 | D. | 减少药品 |
7.下列关于催化剂的说法中,正确的是( )
| A. | 只有二氧化锰能做催化剂 | |
| B. | 催化剂加快反应速率 | |
| C. | 催化剂不能减缓反应速率 | |
| D. | 反应前后催化剂的化学性质不会改变 |
17.VC又名抗坏血酸,人体缺乏VC可能引发许多疾病.某研究性学习小组对它研究如下:
(1)猜想:VC可能具有酸性.
(2)实验方案:请帮助他们把两种实验方案的缺失内容填完整:
(3)结论:VC具有酸性,根据VC的性质,判断下列物质中能与VC反应的是AC
A.Mg B.KCl C.NaOH D.CuSO4
(4)某同学联想到西红柿等蔬菜、水果中含有丰富的维生素C,放置时间长短是否对维生素C的含量产生影响.他设计了如下实验方案:
【查阅资料】①VC能与碘反应.②碘能使淀粉溶液变成蓝色
Ⅰ:把新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液挤入两个烧杯中;
Ⅱ:取两支盛有2mL蓝色碘的淀粉溶液的试管,分别滴加上述两种汁液,边加边振荡,直到蓝色刚好消失,记录滴数如表:
请回答下列问题:
①你认为西红柿中维生素C含量高的是新鲜西红柿的汁液
②你从中得到的启示是西红柿等蔬菜、水果应该食用新鲜的.
(1)猜想:VC可能具有酸性.
(2)实验方案:请帮助他们把两种实验方案的缺失内容填完整:
| 实验内容 | 实验现象 |
| 将维生素C药片研碎,加入蒸馏水配成溶液,取溶液少许注入试管,然后滴入几滴试液,观察现象. | 溶液变成红色,说明维生素C具有酸性. |
| 将维生素C药片研碎,加入蒸馏水配成溶液,再取少许氢氧化钠溶液注入试管并滴入几滴无色酚酞试液,然后逐滴加入维生素C溶液,观察现象. | 如氢氧化钠溶液颜色,说明说明维生素C具有酸性 |
A.Mg B.KCl C.NaOH D.CuSO4
(4)某同学联想到西红柿等蔬菜、水果中含有丰富的维生素C,放置时间长短是否对维生素C的含量产生影响.他设计了如下实验方案:
【查阅资料】①VC能与碘反应.②碘能使淀粉溶液变成蓝色
Ⅰ:把新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液挤入两个烧杯中;
Ⅱ:取两支盛有2mL蓝色碘的淀粉溶液的试管,分别滴加上述两种汁液,边加边振荡,直到蓝色刚好消失,记录滴数如表:
| 汁液 | 新鲜西红柿的汁液 | 放置一周的西红柿的汁液 |
| 滴数 | 12 | 20 |
①你认为西红柿中维生素C含量高的是新鲜西红柿的汁液
②你从中得到的启示是西红柿等蔬菜、水果应该食用新鲜的.
4.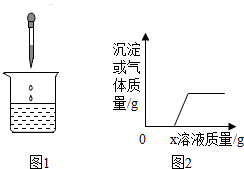 向烧杯中逐滴加入x溶液至过量(图1),生成沉淀或气体的质量与加入溶液的质量关系符合图2的是( )
向烧杯中逐滴加入x溶液至过量(图1),生成沉淀或气体的质量与加入溶液的质量关系符合图2的是( )
 向烧杯中逐滴加入x溶液至过量(图1),生成沉淀或气体的质量与加入溶液的质量关系符合图2的是( )
向烧杯中逐滴加入x溶液至过量(图1),生成沉淀或气体的质量与加入溶液的质量关系符合图2的是( )| 烧杯中的物质 | x溶液 | |
| A | 氯化钠和碳酸氢钠溶液 | 稀盐酸 |
| B | 需硫酸和稀盐酸 | 氯化钡溶液 |
| C | 黄铜粉末 | 稀盐酸 |
| D | 稀盐酸和硫酸镁溶液 | 烧碱溶液 |
| A. | A | B. | B | C. | C | D. | D |
1.用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15克干燥样品进行实验.
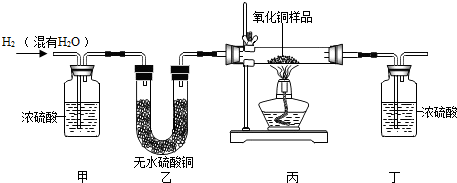
【查阅资料】无水硫酸铜为白色固体,遇水变成蓝色.请根据资料回答:
(1)在实验中,甲装置的作用是除水.
(2)准确称取完全反应前后装置丙和丁的质量如表:
小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度(写出计算过程).
(3)小明根据装置丙的质量变化计算,发现小丽结果偏大.请分析导致这一结果的原因可能是B.
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.氧化铜没有完全被还原.

【查阅资料】无水硫酸铜为白色固体,遇水变成蓝色.请根据资料回答:
(1)在实验中,甲装置的作用是除水.
(2)准确称取完全反应前后装置丙和丁的质量如表:
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
(3)小明根据装置丙的质量变化计算,发现小丽结果偏大.请分析导致这一结果的原因可能是B.
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.氧化铜没有完全被还原.
2.下列微粒的示意图中,表示阳离子的是( )
| A. | 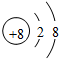 | B. | 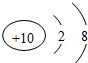 | C. | 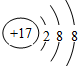 | D. | 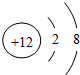 |
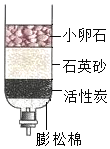 如图是某同学制作的简易净水器,请回答下列问题:
如图是某同学制作的简易净水器,请回答下列问题: