题目内容
10.下列溶液都能跟CuSO4、稀HCl、Na2CO3溶液反应的是( )| A. | Ba(NO3)2 | B. | Ca(OH)2 | C. | H2SO4 | D. | NaOH |
分析 根据题意,选择的物质与CuSO4、稀HCl、Na2CO3溶液均能反应,据此结合盐与酸的化学性质、排除法(只要发现选项中的物质与其中的一种物质不反应,即可排除该选项),进行分析解答.
解答 解:A、Ba(NO3)2与CuSO4反应生成硫酸钡沉淀和硝酸铜,Ba(NO3)2与稀HCl交换成分没有沉淀、气体或水生成,不能发生复分解反应,故选项错误.
B、Ca(OH)2与CuSO4反应生成氢氧化铜沉淀和硫酸钙,与稀盐酸发生中和反应生成氯化钙和水,与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故选项正确.
C、H2SO4与硫酸铜不反应,故选项错误.
D、氢氧化钠与CuSO4反应生成氢氧化铜沉淀和硫酸钠,与稀盐酸发生中和反应生成氯化钠和水,与碳酸钠不反应,故选项错误.
故选:B.
点评 本题难度不大,熟练掌握盐和酸的化学性质是正确解答本题的关键;选用排除法是快速解答的捷径.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列有关资源和能源的叙述中正确的是( )
| A. | 作为高能燃料,目前氢气只被应用于航天领域 | |
| B. | 海洋就是巨大的资源宝库,也是巨大的能源宝库 | |
| C. | 焦炉煤气是煤分馏的产物 | |
| D. | 钠元素不是海水中最多的元素,按元素质量计算,钠元素只排在第三位 |
7.某实验小组开展了如下有关碱的化学性质探究活动:
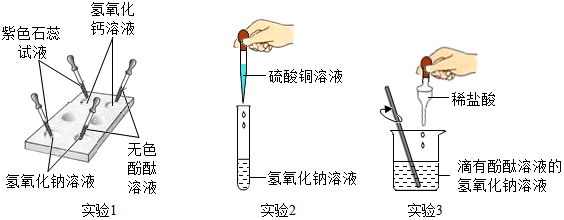
(1)实验2中发生反应的化学方程式是2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
(2)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论.小萍加入的试剂可能是紫色的石蕊试液(或锌粒等).
(3)通过上述实验探究活动,可以总结出碱的化学性质是:
①碱能与酸发生中和反应;
②碱能够和某些盐反应(或碱溶液能够和指示剂反应);
…
(4)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,这两瓶溶液的溶质质量分数分别为5%和10%.请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸).

(1)实验2中发生反应的化学方程式是2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
(2)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论.小萍加入的试剂可能是紫色的石蕊试液(或锌粒等).
(3)通过上述实验探究活动,可以总结出碱的化学性质是:
①碱能与酸发生中和反应;
②碱能够和某些盐反应(或碱溶液能够和指示剂反应);
…
(4)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,这两瓶溶液的溶质质量分数分别为5%和10%.请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸).
| 实验步骤 | 预计现象及相应结论 |
| 取2支洁净的试管,分别加入等体积的两种待测溶液,再分别滴加相同滴数的无色酚酞试液,向溶液中滴加10%的稀盐酸,计算红色刚好消失时所滴加稀盐酸的滴数(或用量) | 红色刚好消失时所滴加稀盐酸的滴数少的为5%的氢氧化钠溶液,另一种为10%的氢氧化钠溶液 |
4.下列有关叙述正确的是( )
| A. | 我国制碱工业的先驱--侯德榜制得的碱是NaOH | |
| B. | 健康人血浆的pH为3.75~4.75 | |
| C. | 草木灰的主要成分是碳酸钾,可为植物补充钾元素,是常见的钾肥 | |
| D. | 尿素和碳酸氢铵是可以长期施用的氮肥,无不良影响 |
5.一氧化氮(NO)是一种无色气体,难溶于水,密度比空气略大,通常情况下极易与氧气反应,生成红棕色的二氧化氮.实验室收集NO的方法是( )
| A. | 向上排空气集气法 | B. | 向下排空气集气法 | ||
| C. | 排水集气法 | D. | 向上排空气集气法和排水集气法 |
 酸碱盐是有广泛用途的重要化合物,某化学活动小组的同学围绕这几类化物合进行了一系探究活动.
酸碱盐是有广泛用途的重要化合物,某化学活动小组的同学围绕这几类化物合进行了一系探究活动.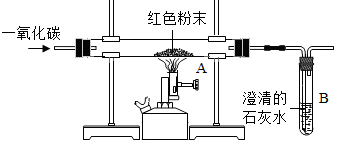 如图是课本中模拟炼铁的实验装置.
如图是课本中模拟炼铁的实验装置.