题目内容
 某化学课外活动小组在实验室配制石灰水时,因发现烧杯底部有固体未溶解,对熟石灰样品的主要成分进行了探究.请你参与讨论并完成实验报告.
某化学课外活动小组在实验室配制石灰水时,因发现烧杯底部有固体未溶解,对熟石灰样品的主要成分进行了探究.请你参与讨论并完成实验报告.【提出问题】针对该熟石灰样品的成分,同学们展开了讨论,小明认为溶解后剩余固体为变质后的难溶性物质,变质的化学方程式为
【进行猜想】猜想一:熟石灰样品成分是Ca(OH)2;
猜想二:熟石灰样品成分是CaCO3;
猜想三:你认为熟石灰样品成分还可能是
【实验与结论】请你通过实验验证你的猜想:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取小烧杯中的物质进行 | 猜想三正确 | |
| ②向①所得液体中加入适量 | 溶液变红 | |
| ③向①所得固体中加入适量稀盐酸 |
①甲组在实验室用pH试纸和配制好的10%盐酸溶液进行实验,实验数据记录见下表.(提示:氯化钙溶液呈中性)
| 加入盐酸溶液的质量/g | 0 | 2.5 | 3.65 | 6 |
| 样品的pH | 12 | 11 | 7 | 2 |
Ⅱ.样品中Ca(OH)2的质量分数是
②乙组同学由计算机描绘出了整个实验过程中溶液pH的变化图象如图.则图中b点溶液中含有的溶质有
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【提出问题】氢氧化钙能和空气中的二氧化碳反应生成碳酸钙和水,氢氧化钙微溶于水;
【进行猜想】样品可能是氢氧化钙和碳酸钙的混合物;
【实验与结论】过滤可以把不溶于水的物质除去;氢氧化钙溶液显碱性,能使酚酞试液变红色;碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
【拓展与应用】①Ⅰ.根据玻璃棒的作用分析;
Ⅱ.根据稀盐酸的质量、溶质质量分数可以计算氢氧化钙的质量,进一步可以计算样品中Ca(OH)2的质量分数.
②溶液的pH、溶液体积、密度质量的计算公式.
【进行猜想】样品可能是氢氧化钙和碳酸钙的混合物;
【实验与结论】过滤可以把不溶于水的物质除去;氢氧化钙溶液显碱性,能使酚酞试液变红色;碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
【拓展与应用】①Ⅰ.根据玻璃棒的作用分析;
Ⅱ.根据稀盐酸的质量、溶质质量分数可以计算氢氧化钙的质量,进一步可以计算样品中Ca(OH)2的质量分数.
②溶液的pH、溶液体积、密度质量的计算公式.
解答:解:【提出问题】熟石灰易于空气中的二氧化碳反应而变质,变质的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
小华同学的理由是氢氧化钙微溶于水,固体还可能是未溶解的氢氧化钙.
【进行猜想】
猜想三:熟石灰样品成分还可能是Ca(OH)2和CaCO3的混合物.
【实验与结论】
①取小烧杯中的物质进行过滤,得到固体和液体;
②向①所得液体中加入适量酚酞溶液,溶液变红;
③向①所得固体中加入适量稀盐酸,有气泡产生;
【拓展与应用】
Ⅰ.边滴加稀盐酸,边不断搅拌的目的是使反应物充分接触充分反应;
Ⅱ.设:样品中Ca(OH)2的质量为x,
Ca(OH)2+2HCl=CaCl2+2H2O,
74 73
x 3.65g×10%
=
解得:x=0.37g,
样品中Ca(OH)2的质量分数为:
×100%=74%,
②由图象可知,则图中b点溶液的pH小于7,溶液呈酸性,说明加入的盐酸过量,溶液的溶质有生成的氯化钙和剩余的盐酸,化学式是:HCl、CaCl2;已知盐酸的体积,要求盐酸的质量还要知道密度.
故答为:【提出问题】Ca(OH)2+CO2=CaCO3↓+H2O;氢氧化钙微溶于水,未溶解的固体还有可能是氢氧化钙;
【进行猜想】Ca(OH)2和CaCO3;
【实验与结论】过滤,酚酞;产生大量的气泡;
【拓展与应用】①Ⅰ.使反应物充分接触充分反应;Ⅱ.74%;②HCl、CaCl2;该盐酸的密度.
小华同学的理由是氢氧化钙微溶于水,固体还可能是未溶解的氢氧化钙.
【进行猜想】
猜想三:熟石灰样品成分还可能是Ca(OH)2和CaCO3的混合物.
【实验与结论】
①取小烧杯中的物质进行过滤,得到固体和液体;
②向①所得液体中加入适量酚酞溶液,溶液变红;
③向①所得固体中加入适量稀盐酸,有气泡产生;
【拓展与应用】
Ⅰ.边滴加稀盐酸,边不断搅拌的目的是使反应物充分接触充分反应;
Ⅱ.设:样品中Ca(OH)2的质量为x,
Ca(OH)2+2HCl=CaCl2+2H2O,
74 73
x 3.65g×10%
| 74 |
| 73 |
| x |
| 3.65g×10% |
样品中Ca(OH)2的质量分数为:
| 0.37g |
| 0.5g |
②由图象可知,则图中b点溶液的pH小于7,溶液呈酸性,说明加入的盐酸过量,溶液的溶质有生成的氯化钙和剩余的盐酸,化学式是:HCl、CaCl2;已知盐酸的体积,要求盐酸的质量还要知道密度.
故答为:【提出问题】Ca(OH)2+CO2=CaCO3↓+H2O;氢氧化钙微溶于水,未溶解的固体还有可能是氢氧化钙;
【进行猜想】Ca(OH)2和CaCO3;
【实验与结论】过滤,酚酞;产生大量的气泡;
【拓展与应用】①Ⅰ.使反应物充分接触充分反应;Ⅱ.74%;②HCl、CaCl2;该盐酸的密度.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
下列化学知识的总结正确的是( )
①酒精挥发是其物理性质
②石油液化气燃烧是其化学性质
③食用加碘盐可以预防人体贫血
④木柴架空有利于木柴的完全燃烧
⑤蔬菜能为人体提供多种维生素
⑥用细沙灭火降低了可燃物着火点.
①酒精挥发是其物理性质
②石油液化气燃烧是其化学性质
③食用加碘盐可以预防人体贫血
④木柴架空有利于木柴的完全燃烧
⑤蔬菜能为人体提供多种维生素
⑥用细沙灭火降低了可燃物着火点.
| A、①②④⑤ | B、②③④⑤ |
| C、③④⑤⑥ | D、①③④⑥ |
2014年“6.5”世界环境日中国主题:“向污染宣战”.下列做法不符合该主题的是( )
| A、达标排放工业废水 |
| B、就地焚烧生活垃圾 |
| C、开发和使用新能源 |
| D、大力开展植树造林 |
实验需要10%的氢氧化钠溶液50g,配制溶液时不正确的是( )
| A、实验步骤是计算、称量(量取)、溶解、装瓶、贴标签 |
| B、用50mL量筒量取所需水的体积 |
| C、实验中用到的玻璃仪器有烧杯、量筒、玻璃棒 |
| D、俯视读数,这样配得的溶液浓度会偏高 |
下列实验操作不能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去混入氮气中的氧气 | 通过炽热的铜网 |
| B | 检验二氧化碳中含有少量的一氧化碳 | 点燃 |
| C | 鉴别氯化钙和碳酸钙 | 加入足量的水 |
| D | 检验黄铜中含有锌 | 加入稀盐酸 |
| A、A | B、B | C、C | D、D |
小明在资料中找到下列微粒的结构示意图,请你分析以下的叙述中正确的是( )
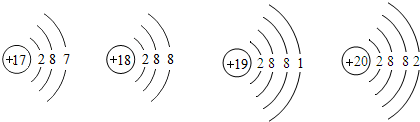

| A、上述各微粒中,最外层电子数都没有达到稳定结构 |
| B、核电荷数为18的微粒是失电子后形成的阴离子 |
| C、原子序数为19的元素的金属活动性,比原子序数为20的元素的金属活动性强 |
| D、质子数为17、18的微粒都属于易得电子的非金属元素 |
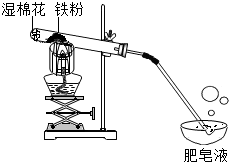 钢铁在生产生活中具有广泛用途.
钢铁在生产生活中具有广泛用途.

