题目内容
6.通过一年的化学学习,你己经掌握了实验室制取气体的有关规律.请结合如图提供的一些实验装置回答问题:
(1)若用A装置制取氧气,仪器a中需加入过氧化氢发生的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氮水.当你选用加热氯化按和氢氧化钙的固体混合物来制取氨气时,若选择 B 装置来完成该实验,需进行的改动是使试管口略向下倾斜;用酒精灯加热. 反应的方程式为:2NH4Cl+Ca(OH)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)你认为应选择收集氨气的装置最好是F(填序号),原因是用水吸收氨气,防止氨气扩散到空气中,减少污染,同时利用氨气极易溶于水的性质来验满.
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(2)根据题目中的信息“加热氯化铵和氢氧化钙的固体混合物来制取氨气”,进行书写化学方程式,发生装置主要由反应物的状态和反应条件决定;
(3)收集装置主要由气体的密度和溶水性决定.
解答 解:(1)若用A装置制取氧气,应该是利用过氧化氢制取氧气,仪器a中需加入过氧化氢,化学式是H2O2;发生反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)根据题目中的信息“加热氯化铵和氢氧化钙的固体混合物来制取氨气”,则氯化铵和氢氧化钙在加热条件下反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;若选择B装置来完成该实验,需进行的改动 使试管口略向下倾斜;用酒精灯加热.
(3)因为氨气会污染空气,故收集氨气的装置最好是F装置,原因是 用水吸收氨气,防止氨气扩散到空气中,减少污染,同时利用氨气极易溶于水的性质来验满.
故答案为:
(1)过氧化氢,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(2)使试管口略向下倾斜;用酒精灯加热 2NH4Cl+Ca(OH)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
(3)F 用水吸收氨气,防止氨气扩散到空气中,减少污染,同时利用氨气极易溶于水的性质来验满
点评 本道题主要考查了实验室制取气体发生装置和收集装置的选取,发生装置主要由反应物的状态和反应条件决定,收集装置主要由气体的密度和溶水性决定,另外还要考虑气体是否与水反应、是否与空气反应、是否有毒等等.

 阅读快车系列答案
阅读快车系列答案 下列各组物质间通过一步反应就能实现如图转化,则X、Y、Z可能的组合是( )
下列各组物质间通过一步反应就能实现如图转化,则X、Y、Z可能的组合是( )| X | Y | Z | |
| A | Fe | FeCl2 | Fe2O3 |
| B | Ca(OH)2 | NaOH | NaCl |
| C | AgNO3 | Ba(NO3)2 | BaSO4 |
| D | H2O | O2 | CO2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | ● | B. | ○ | C. | ●● | D. |  |
 (如图)这里的钙、镁、钾、钠指的是( )
(如图)这里的钙、镁、钾、钠指的是( )| A. | 原子 | B. | 分子 | C. | 单质 | D. | 元素 |
| A. | 在花园中可闻到花香--分子在不断运动 | |
| B. | 用肉眼不能直接观察到水分子--水分子很小 | |
| C. | 50毫升水与50毫升酒精混合后总体积小于100毫升--分子之间有间隔 | |
| D. | 冰受热变为水,水受热变为水蒸气--分子可以再分 |
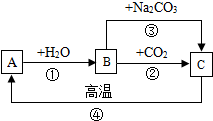 A、B、C是三种含有同一种金属元素的化合物.它们之间有如图所示的转化关系(部分产物略去).
A、B、C是三种含有同一种金属元素的化合物.它们之间有如图所示的转化关系(部分产物略去).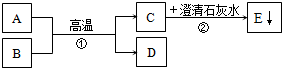 已知A为黑色固体,D为金属单质.A、B、C、D、E五种物质之间的转化关系如图所示.请回答:
已知A为黑色固体,D为金属单质.A、B、C、D、E五种物质之间的转化关系如图所示.请回答:
