题目内容
14.如图是甲烷燃烧的微观模拟图,请回答下列问题:
(1)在点燃的条件下,A到B的过程表示的是甲烷分子分解成碳原子和氢原子,氧分子分解成氧原子,请简述B到C的过程;
(2)写出该反应的化学方程式.
分析 (1)由微观模拟图可知,图B中的碳、氢、氧原子重新结合成图C中的二氧化碳分子和水分子;
(2)由微观模拟图A、C可得知,每个甲烷分子与两个氧分子反应,生成两个水分子和一个二氧化碳分子,据此可写出反应的化学方程式.
解答 解:(1)图B中的每2个H原子与1个O原子结合成水分子,每个C原子与2个O原子结合成二氧化碳分子;
故答案为:一个碳原子和两个氧原子结合成二氧化碳分子,一个氧原子和两个氢原子结合成一个水分子;
(2)该反应为每个甲烷分子与两个氧分子反应,生成两个水分子和一个二氧化碳分子,故反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
点评 本题是有关微观示意图的考查,依据化学变化的实质为分子$\stackrel{分成}{→}$原子$\stackrel{重新组合}{→}$分子,变化过程中原子不变,只是原子重新结合成新的分子的过程.

练习册系列答案
相关题目
6.将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{O_{2}}{→}$ 钠的氧化物 $\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$ 白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH; 2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O 猜想2:Na2O2 猜想3:Na2O和Na2O2
【实验探究一】:
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】猜想一:Na2CO3猜想二:Na2CO3和NaOH
【实验探究二】:
【实验反思】
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl═4NaCl+2H2O+X,X的化学式为O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
钠(Na)$\stackrel{O_{2}}{→}$ 钠的氧化物 $\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$ 白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH; 2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O 猜想2:Na2O2 猜想3:Na2O和Na2O2
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 无气泡生成 | 猜想1正确 |
【作出猜想】猜想一:Na2CO3猜想二:Na2CO3和NaOH
【实验探究二】:
| 实验操作 | 实验现象 | 实验结论 |
| 1、取少量白色固体加入足量CaCl2溶液. | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2、过滤、取少量滤液加入 无色酚酞试液 | 试液变红 |
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl═4NaCl+2H2O+X,X的化学式为O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
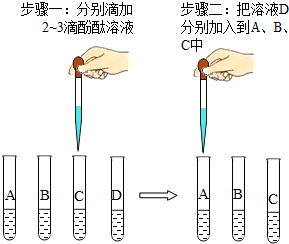 在实验台上有四瓶未贴标签的溶液,已知分別是碳酸钾溶液、氯化钠溶液、氯化钡溶液和稀硫酸.为了鉴别这四种溶液,在老师的指导下,兴趣小组的同学把这四种溶液按A、B、C、D进行编号,分别各取适量作为样品加入到四支试管中,进行了如图所示的探究活动:
在实验台上有四瓶未贴标签的溶液,已知分別是碳酸钾溶液、氯化钠溶液、氯化钡溶液和稀硫酸.为了鉴别这四种溶液,在老师的指导下,兴趣小组的同学把这四种溶液按A、B、C、D进行编号,分别各取适量作为样品加入到四支试管中,进行了如图所示的探究活动: