题目内容
20.将碳酸钠和氯化钠的固体混合物17g放入烧杯中,加100g水完全溶解,加入50g稀盐酸,恰好完全反应,待没有气泡逸出后再次称量(CO2的溶解忽略不计),总质量为164.8g.计算:所得溶液中溶质的质量分数.(计算结果保留至0.1%)分析 根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算碳酸钠和生成的氯化钠的质量,进而求算对应的质量分数.
解答 解:根据质量守恒定律可得,生成的二氧化碳的质量为17g+100g+50g-164.8g=2.2g
设参加反应的碳酸钠的质量为x,生成的氯化钠的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 2.2g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{2.2g}$
x=5.3g
y=5.85g
所得溶液中溶质的质量分数为$\frac{17g-5.3g+5.85g}{164.8g}$×100%≈10.6%
答:所得溶液中溶质的质量分数约为10.6%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
11.“水是生命之源”,有关水的认识正确的是( )
| A. | 电解水得到H2和O2,可知水是由氢气和氧气组成的 | |
| B. | 生活中用过滤的方法可以降低水的硬度 | |
| C. | 净水的方法有沉淀、过滤、吸附、蒸馏等 | |
| D. | 氢氧化钠、氯化钠、硝酸铵分别加入一定量水中形成溶液后温度一定会升高或下降 |
9. (1)以下是有关CO2气体溶解度的几组数据:
(1)以下是有关CO2气体溶解度的几组数据:
CO2在水中的溶解度(单位:mL)
①根据CO2在水中的溶解度表,叙述外界条件是如何影响气体溶解度的?
温度升高,气体的溶解度减小、压强增大,气体的溶解度增大.
②打开可乐瓶有气体溢出,说明原瓶中的压强大于(填:大于、小于或等于)瓶外大气压强.
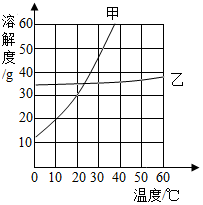
(2)如图是无结晶水合物的固体甲和乙在水中的溶解度曲线,请根据该曲线图回答下列问题:
①20°C时,150g水中溶解45g甲物质才能形成饱和溶液.
②现有60℃的乙的饱和溶液,与该溶液有关的量有:
A.水的质量
B.溶液中溶质的质量
C.溶液的质量
D.乙的质量分数
E.60℃时乙的溶解度
保持温度不变,将该饱和溶液稀释,不变的量是BE(填序号,下同);如果将该饱和溶液降温至20℃,不变的量是AE.
 (1)以下是有关CO2气体溶解度的几组数据:
(1)以下是有关CO2气体溶解度的几组数据:CO2在水中的溶解度(单位:mL)
| 压强/大气压 | 温度/℃ | ||||
| 0 | 25 | 50 | 75 | 100 | |
| 1 | 1.79 | 0.752 | 0.423 | 0.307 | 0.231 |
| 10 | 15.92 | 7.14 | 4.095 | 2.99 | 2.28 |
| 25 | 29.30 | 16.20 | 9.71 | 6.82 | 5.73 |
温度升高,气体的溶解度减小、压强增大,气体的溶解度增大.
②打开可乐瓶有气体溢出,说明原瓶中的压强大于(填:大于、小于或等于)瓶外大气压强.
(2)如图是无结晶水合物的固体甲和乙在水中的溶解度曲线,请根据该曲线图回答下列问题:
①20°C时,150g水中溶解45g甲物质才能形成饱和溶液.
②现有60℃的乙的饱和溶液,与该溶液有关的量有:
A.水的质量
B.溶液中溶质的质量
C.溶液的质量
D.乙的质量分数
E.60℃时乙的溶解度
保持温度不变,将该饱和溶液稀释,不变的量是BE(填序号,下同);如果将该饱和溶液降温至20℃,不变的量是AE.
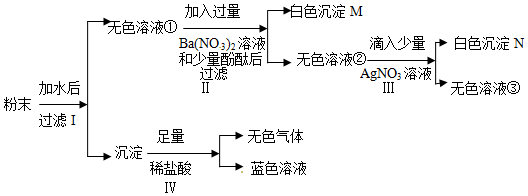
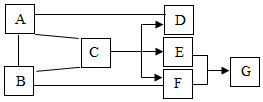 A~G是初中化学中常见的七种物质,其中A、B、C、E、F、G含有同一种元素,A、B、C、E、G是五种不同类别的物质;D和F在通常情况下为气体,两者分别溶于水后溶液的酸碱性相反.它们相互间的关系如图所示.(图中“-”表示相连的物质之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件己略去.)
A~G是初中化学中常见的七种物质,其中A、B、C、E、F、G含有同一种元素,A、B、C、E、G是五种不同类别的物质;D和F在通常情况下为气体,两者分别溶于水后溶液的酸碱性相反.它们相互间的关系如图所示.(图中“-”表示相连的物质之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件己略去.)
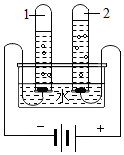 电解水实验如图所示.
电解水实验如图所示.