题目内容
5.有一包粉末,已知其由BaCO3、Cu(NO3)2、Na2SO4、NaCl、NaOH中的几种组成,现对其做以下实验,各步骤均已经充分反应,请回答问题: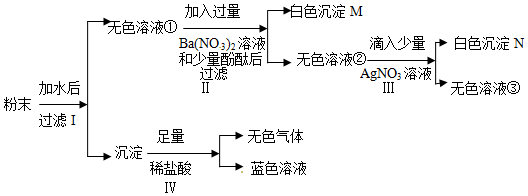
(1)请写出沉淀N的化学式:AgCl.
(2)步骤Ⅱ所发生反应的化学方程式为Na2SO4+Ba(NO3)2═BaSO4+2NaNO3,其基本反应类型为复分解反应.
(3)无色溶液②中一定存在的溶质(酚酞除外)的化学式为NaCl、NaNO3、Ba(NO3)2.
(4)这包粉末中共含有五种物质.
分析 根据题干提供的信息进行分析解答,粉末加水得到的是无色溶液和沉淀,且沉淀加入足量的稀盐酸能得到气体和蓝色溶液,故得到的沉淀中含有氢氧化铜沉淀和碳酸钡沉淀,一定含有碳酸钡、氢氧化钠和硝酸铜;得到的无色溶液①加入硝酸钡产生白色沉淀,故沉淀M是硫酸钡,说明一定含有硫酸钠;无色滤液②中佳人苑硝酸银产生白色沉淀,故生成的沉淀N是氯化银,据此解答.
解答 解:粉末加水得到的是无色溶液和沉淀,且沉淀加入足量的稀盐酸能得到气体和蓝色溶液,故得到的沉淀中含有氢氧化铜沉淀和碳酸钡沉淀,一定含有碳酸钡、氢氧化钠和硝酸铜;得到的无色溶液①加入硝酸钡产生白色沉淀,故沉淀M是硫酸钡,说明一定含有硫酸钠;无色滤液②中佳人苑硝酸银产生白色沉淀,故生成的沉淀N是氯化银;
(1)N是氯化银,故填:AgCl;
(2)步骤Ⅱ中硫酸钠与硝酸钡反应生成硫酸钡沉淀和硝酸钠,属于复分解反应,故填:Na2SO4+Ba(NO3)2═BaSO4+2NaNO3;复分解反应;
(3)无色溶液②中一定存在过量的硝酸钡、氯化钠和生成的硝酸钠,故填:NaCl、NaNO3、Ba(NO3)2;
(4)经过推断,这包粉末中一定含有氢氧化钠、硝酸铜、碳酸钡、硫酸钠和氯化钠五种物质,故填:五.
点评 本题考查的是常见的混合物成分的推断,完成此题,可以依据已有的物质的性质以及物质间反应的实验现象进行.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
12.2017年5月18日,国土资源部宣布:我国首次(也是世界首次)在南海成功试采海域可燃冰.可燃冰的主要成分是( )
| A. | 甲烷水合物 | B. | 一氧化碳 | C. | 氢气 | D. | 氮气 |
13.图中字母代表含硫元素的物质,下列判断错误的是( ) 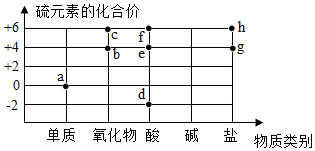

| A. | 物质a在纯氧气中燃烧可以生成物质b | |
| B. | 物质c是二氧化碳 | |
| C. | 物质d中硫元素的化合价为-2价 | |
| D. | 物质d、e和f中一定都含有氢元素 |
10.下列归纳和总结完全正确的一组是( )
| A、对鉴别的认识 | B、对安全的认识 |
| ①区分硬水和软水,加肥皂水后搅拌 ②区分棉纤维和羊毛纤维,点燃后闻气味 ③区分硫酸铵和硫酸钾,加熟石灰研磨 | ①在室内放一盆水能防止煤气中毒 ②档案室着火用二氧化碳灭火器灭火 ③进入地窖前先做灯火实验 |
| C、对化学与生活的认识 | D、对材料科学的认识 |
| ①洗涤剂去油污是因为起乳化作用 ②植物叶子发黄,说明植物要补充磷肥 ③使煤燃烧更旺--把煤做成蜂窝煤 | ①聚乙烯、合成纤维都属于合成材料 ②生铁、金刚石都属于金属材料 ③玻璃钢、不锈钢都属于复合材料 |
| A. | A | B. | B | C. | C | D. | D |