题目内容
5. 铝、铁、铜是人类广泛使用的三种金属,回答下列问题.
铝、铁、铜是人类广泛使用的三种金属,回答下列问题.(1)在空气中,铝制品抗腐蚀较强的原因是铝与氧气反应生成氧化铝,在铝的表面会形成一层致密的氧化膜,保护内层金属不被进一步氧化;
(2)用稀硫酸验证这三种金属的活动性顺序,将足量三种金属片依次放入烧杯中并使之充分反应,能实现目的是BC;
A.铝、铁、铜 B.铁、铜、铝 C.铜、铁、铝
(3)合金具有比纯金属更多的优良性能,如钢比纯铁硬度大,应用更广泛.
分析 (1)根据铝制品易与氧气反应生成一层致密的氧化膜;(2)根据金属与酸反应的条件考虑;(3)根据合金比组成成分金属的硬度大、熔点低考虑.
解答 解:(1)铝与氧气反应生成氧化铝,在铝的表面会形成一层致密的氧化膜,保护内层金属不被进一步氧化;
(2)由于金属片是足量的所以能与硫酸反应金属都会把硫酸反应完,A答案中铝与硫酸生成了硫酸铝,再加入铁和铜时,铁和铜都不能与硫酸铝反应,所以不能排出铁和铜的顺序,故A错;B答案中铁与硫酸反应生成了硫酸亚铁,再加入铜,由于铜与硫酸亚铁不反应,所以铜排在铁的后面,再加入铝,铝能与硫酸亚铁反应,所以铝排在铁的前边,所以能排出三种金属的活动性顺序,故B正确;C加入铜,由于铜不能与硫酸反应,所以铜排在氢的后面,再加入铁,铁与硫酸反应生成硫酸亚铁和氢气,所以铁排在氢的前边,即铁排在铜的前边,再加入铝,铝能与硫酸亚铁反应,说明铝排在铁的前边,所以能排出三种金属的活动性顺序,故D答案正确.
(3)合金比组成成分金属的硬度大、熔点低.
故答案为:(1)铝与氧气反应生成氧化铝,在铝的表面会形成一层致密的氧化膜,保护内层金属不被进一步氧化;(2)BC;(3)大.
点评 解答本题关键是要熟悉金属与酸反应的条件:金属要排在氢的前边,酸不能是浓硫酸和硝酸,合金比组成成分金属的硬度大、熔点低、耐腐蚀性强.

练习册系列答案
相关题目
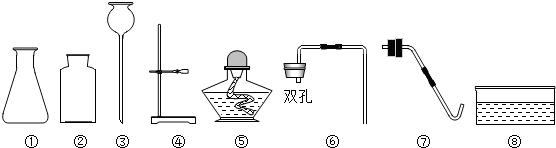
15.欲配制100g质量分数为10%的氯化钠溶液,一定能用到的仪器组合是( )
①托盘天平 ②烧杯 ③玻璃棒 ④50ml量筒.
①托盘天平 ②烧杯 ③玻璃棒 ④50ml量筒.
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | ①②③④ |
16.传统腌制松花蛋的主要配料是氧化钙、纯碱和食盐.某活动小组将这三种物质混合后加入适量水搅拌、过滤后,对滤液中溶质的成分进行探究:
(1)【猜想与假设】
甲同学猜想:可能是NaCl、Ca(OH)2、Na2CO3
乙同学猜想:可能是NaCl、NaOH、Na2CO3
丙同学猜想:可能是NaCl、Ca(OH)2、NaOH
丁同学猜想:可能是NaCl、NaOH
【交流与评价】大家一致认为甲同学的猜想不成立,理由一是:Ca(OH)2和Na2CO3能反应而不能共存,理由二是:没有氢氧化钙和碳酸钠反应生成的氢氧化钠
(2)【活动与探究】
(3)【解释与结论】丁同学的结论是否正确不正确.丁同学和乙同学使用了相同的试剂,却没有看到气泡产生,你认为可能的原因是:少量的盐酸只能够和氢氧化钠反应生成碳酸钠和水.
(1)【猜想与假设】
甲同学猜想:可能是NaCl、Ca(OH)2、Na2CO3
乙同学猜想:可能是NaCl、NaOH、Na2CO3
丙同学猜想:可能是NaCl、Ca(OH)2、NaOH
丁同学猜想:可能是NaCl、NaOH
【交流与评价】大家一致认为甲同学的猜想不成立,理由一是:Ca(OH)2和Na2CO3能反应而不能共存,理由二是:没有氢氧化钙和碳酸钠反应生成的氢氧化钠
(2)【活动与探究】
| 实验步骤 | 实验现象及相关化学方程式 | 实验结论 |
| 乙同学取一定量的滤液于试管中,向其中加入一定量的盐酸 | 有大量气泡生成,写出产生气泡的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑ | 乙同学的猜想成立 |
丙同学取一定量的滤液于试管中,向其中加入一定量的碳酸钠溶液 | 实验现象产生白色沉淀 | 丙同学的猜想成立 |
| 丁同学取一定量的滤液于试管中,向其中滴加少量盐酸. | 无气泡产生 | 乙同学猜想不成立 |
20.如图所示的实验操作,正确的是( )
| A. |  闻气体气味 | B. |  取用块状固体 | C. |  加热液体 | D. |  读液体体积数 |
17.下列验证质量守恒定律的实验中,得出正确结论的是( )
| A. |  蜡烛燃烧前后质量的测定 | |
| B. |  镁条燃烧前后质量的测定 | |
| C. |  石灰石和稀盐酸反应前后质量的测定 | |
| D. |  白磷燃烧前后质量的测定 |
14.下列物质的性质与所对应的用途没有直接关系的是( )
| A. | 氧气的密度比空气略大--用于急救病人 | |
| B. | 氮气的性质稳定--作焊接保护气 | |
| C. | 稀有气体通电发光--制作电光源 | |
| D. | 干冰升华吸热--用于人工降雨 |
15. 请你根据生活经验及所学的知识,结合实验回答下列问题:
请你根据生活经验及所学的知识,结合实验回答下列问题:
(1)某校化学课外小组的同学,利用塑料瓶(质软)设计了下图所示的实验.
①请你分析并推测振荡后塑料瓶将发生什么变化?塑料瓶变瘪.
②发生该变化的原因是:二氧化碳溶于水,瓶内压强减小,大气压把塑料瓶压瘪.
(2)甲同学把瓶盖打开,滴入紫色石蕊溶液,发现溶液变红色,他们随即进行探究:
【猜想】①是水使石蕊变红.②是CO2使石蕊变红.③是CO2与水反应生成的新物质使石蕊变红.
【设计方案并进行实验】
乙同学认为还要做水能否使石蕊变红的对比实验,你认为有没有必要?为什么?没有必要;因为石蕊溶液中有水,证明水不能使石蕊变红.
 请你根据生活经验及所学的知识,结合实验回答下列问题:
请你根据生活经验及所学的知识,结合实验回答下列问题:(1)某校化学课外小组的同学,利用塑料瓶(质软)设计了下图所示的实验.
①请你分析并推测振荡后塑料瓶将发生什么变化?塑料瓶变瘪.
②发生该变化的原因是:二氧化碳溶于水,瓶内压强减小,大气压把塑料瓶压瘪.
(2)甲同学把瓶盖打开,滴入紫色石蕊溶液,发现溶液变红色,他们随即进行探究:
【猜想】①是水使石蕊变红.②是CO2使石蕊变红.③是CO2与水反应生成的新物质使石蕊变红.
【设计方案并进行实验】
| 实验操作步骤 | 实验现象 | 结论 |
| 把用石蕊溶液染成紫色的干燥纸花放入盛有干燥二氧化碳的集气瓶中 | 纸花不变红 | 猜想②不正确 |
| 把用石蕊溶液染成紫色的干燥纸 花先喷水,然后放入盛有二氧化碳的集气瓶中 | 纸花变红 | 猜想③正确 |
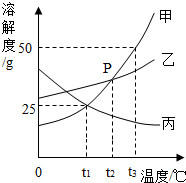 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列问题:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列问题: