题目内容
8. 质量守恒定律的定量研究对化学科学发展具有重大意义.
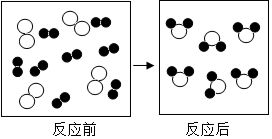
质量守恒定律的定量研究对化学科学发展具有重大意义.(1)如图是某反应的微观示意图(其中“○”和“
 ”分别表示不同的原子).
”分别表示不同的原子).①反应后方框内应再填入2个“
 ”微粒.
”微粒.②请从微观的角度分析化学变化的实质是反应物的原子再重新组合成新物质的分子过程.
(2)在一密闭容器内有4种物质A、B、C、D,它们在一定条件下发生化学反应.其中A、B、C的微观示意图和反应前后各物质的质量如下表所示.
| 物质 | A | B | C | D |  |
| 微观示意图 |  |  |  | ||
| 反应前质量/g | 100 | 1 | 1 | 46 | |
| 反应后质量/g | 4 | 55 | 89 | x |
②若D的相对分子质量为46,该反应的化学方程式是C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
分析 (1)①根据质量守恒定律反应前后原子的种类及数目不变分析;
②根据反应的微观示意图中微粒的变化分析化学变化的实质;
(2)①根据质量守恒定律,由物质质量的增减量可确定反应物和生成物的质量,从而得出X的值;
②根据物质中元素的质量可确定构成物质的原子个数比,从而得到物质的化学式,根据化学方程式的书写步骤可写出该反应的化学方程式.
解答 解:(1)①由质量守恒定律反应前后原子的种类及数目不变可知,反应后方框内应生成8个 微粒,现已有了6个,应再添加2个
微粒,现已有了6个,应再添加2个 .
.
②由反应的微观示意图中微粒的变化可知化学变化的实质是:反应物的原子再重新组合成新物质的分子过程;
(2)①由质量守恒定律及由表中数据可知:二氧化碳的质量增加了89g-1g=88g,可确定二氧化碳是生成物;水蒸气的质量增加了55g-1g=54g,可确定水蒸气是生成物;氧气的质量减少了100g-4g=96g<88g+54g,可确定氧气和D都是反应物.D减少的质量为:88g+54g-96g=46g,因此X的值为:46-46=0.
②因反应物中的氧气里只含氧元素,因此生成物中的碳元素和氢元素一定来自D,即D中一定含有碳、氢两元素,生成物中氧元素的质量为88g×$\frac{16×2}{44}$+54g×$\frac{16}{18}$=112g>96g,可确定生成物中的一部分氧元素来自D,即D中一定含有氧元素,D中碳、氢、氧三元素的原子个数比为:$\frac{88g×\frac{12}{44}}{12}$:$\frac{54g×\frac{1×2}{18}}{1}$:$\frac{112g-96g}{16g}$=2:6:1,故D的化学式为C2H6O,该反应的化学方程式为:C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
故答为:(1)①2,②反应物的原子再重新组合成新物质的分子过程;(3)0,C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
点评 此题是对化学反应的微观过程的考查,解题的关键是依据已有的化学反应实质和结合图示物质的结构进行.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 物质都是由元素组成的 | |
| B. | 原子序数等于该元素原子核内的质子数 | |
| C. | 元素既论种又论个 | |
| D. | 在化学变化中元素的种类不发生改变 |
| A. | Fe | B. | O2 | C. | O2- | D. | H2O |
| A. | 在点燃条件下,质量比为1:1的硫和氧气恰好完全化合成二氧化硫 | |
| B. | 在点燃条件下,质量比为1:2的碳和氧气恰好完全化合成二氧化碳 | |
| C. | 在点燃条件下,分子个数比为2:1的氢气和氧气恰好完全化合成水 | |
| D. | 在反应3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4中,Fe、O2、Fe3O4三种物质的质量比为168:64:232 |
| A. | 2毫升 | B. | 3毫升 | C. | 5毫升 | D. | 6毫升 |




 “微粒运动实验”再探究.
“微粒运动实验”再探究.