题目内容
20.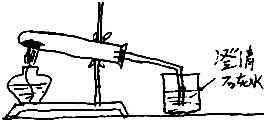 某同学对课本加热铜绿的实验改为如图所示进行,请回答下列问题:
某同学对课本加热铜绿的实验改为如图所示进行,请回答下列问题:(1)该实验中可观察到的现象有绿色粉末受热后变成黑色,澄清的石灰水变浑浊,试管壁有水珠
(2)铜在潮湿空气中,与氧气、水、二氧化碳常温下反应生成铜绿.请写出该反应的文字表达式:碱式碳酸铜$\stackrel{加热}{→}$氧化铜+水+二氧化碳
(3)根据上述信息,铜在实验室该如何保存?密封保存
(4)实验中试管口略向下倾斜的原因是防止冷凝的水倒流回试管底部引起试管炸裂
(5)实验结束后,应该先撤导管,后撤酒精灯,这是为了防止水倒吸,炸裂试管.
分析 (1)根据碱式碳酸铜加热生成氧化铜、水和二氧化碳进行分析;
(2)根据碱式碳酸铜在加热的条件下生成氧化铜、水和二氧化碳进行分析;
(3)根据铜会与空气中的水、二氧化碳、氧气反应而发生锈蚀进行分析;
(4)试管口略向下倾斜的目的是防止冷凝的水倒流回试管底部引起试管炸裂;
(4)根据熄灭酒精灯后试管内气压变小,石灰水会沿导管倒流入试管导致试管破裂解答.
解答 解:(1)碱式碳酸铜加热生成氧化铜、水和二氧化碳,氧化铜是黑色固体,二氧化碳能使澄清的石灰水变浑浊,所以观察到的现象为:绿色粉末受热后变成黑色,澄清的石灰水变浑浊,试管壁有水珠;
(2)碱式碳酸铜在加热的条件下生成氧化铜、水和二氧化碳,文字表达式为:碱式碳酸铜$\stackrel{加热}{→}$氧化铜+水+二氧化碳;
(3)铜会与空气中的水、二氧化碳、氧气反应而发生锈蚀,所以铜在实验室应该密封保存;
(4)试管口略向下倾斜的目的是防止冷凝的水倒流回试管底部引起试管炸裂;
(4)熄灭酒精灯后试管内气压变小,石灰水会沿导管倒流入试管导致试管破裂.
故答案为:(1)绿色粉末受热后变成黑色,澄清的石灰水变浑浊,试管壁有水珠;
(2)碱式碳酸铜$\stackrel{加热}{→}$氧化铜+水+二氧化碳;
(3)密封保存;
(4)防止冷凝的水倒流回试管底部引起试管炸裂;
(4)导管,酒精灯,防止水倒吸,炸裂试管.
点评 掌握碱式碳酸铜受热分解生成氧化铜、水和二氧化碳是解题的关键.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
10.下列物质属于纯净物的是 ( )
| A. | 生铁 | B. | 黄铜 | C. | 不锈钢 | D. | 干冰 |
11.关于物质的组成、结构和性质的关系归纳错误的是( )
| A. | 物质是由分子、原子、离子等粒子构成 | |
| B. | 原子是化学反应中的最小粒子,因此原子不可再分 | |
| C. | 核内质子数决定了元素的种类 | |
| D. | 元素的化学性质与原子的最外层电子数关系密切 |
5.学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:氧化铜(CuO)能否起到类似MnO2的催化作用呢?于是进行了以下探究.
【猜想】
Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图1的实验:
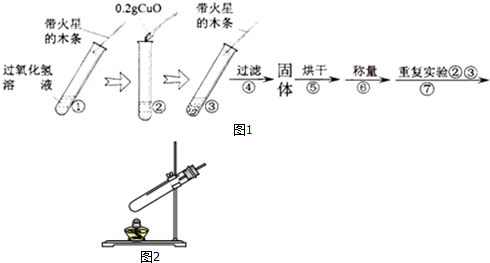
(1)填写下表:
(2)步骤①(填序号)的目的是证明CuO能加快过氧化氢溶液分解的速率;
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)步骤⑦的目的是证明氧化铜的化学性质在反应前后没有发生改变.
(5)过氧化氢能被CuO催化分解放出O2的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(6)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
【猜想】
Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图1的实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 剧烈反应,产生大量气泡 带火星的木条复燃 | 0.2g | 溶液中有气泡放出 带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)步骤⑦的目的是证明氧化铜的化学性质在反应前后没有发生改变.
(5)过氧化氢能被CuO催化分解放出O2的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(6)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体存在,其化学式为Ca10(PO4)6(OH)2.如图是某牛奶包装盒的部分文字,请你仔细阅读后
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体存在,其化学式为Ca10(PO4)6(OH)2.如图是某牛奶包装盒的部分文字,请你仔细阅读后
 11月24日杭州地铁1号线正式开通,目前共设车站31座,两次穿越钱塘江、四次越过京杭大运河,是全球第一条覆盖有4G网络的地铁线路.该条地铁系统以高度人性化和细腻清新的江南风格著称.地铁是近年来新兴的城市地下交通工具,动力为电力,开动时电车上裸露的电刷沿架空电线滑动.当它开动时,跟架空电线的接触点上,由于高速摩擦,会产生高温.它应该具有耐高温,不易氧化,能导电的性质.
11月24日杭州地铁1号线正式开通,目前共设车站31座,两次穿越钱塘江、四次越过京杭大运河,是全球第一条覆盖有4G网络的地铁线路.该条地铁系统以高度人性化和细腻清新的江南风格著称.地铁是近年来新兴的城市地下交通工具,动力为电力,开动时电车上裸露的电刷沿架空电线滑动.当它开动时,跟架空电线的接触点上,由于高速摩擦,会产生高温.它应该具有耐高温,不易氧化,能导电的性质.