题目内容
14.“催化转换器”可将汽车尾气中有毒气体转化为无毒气体,如图是其中一个转化的微观过程.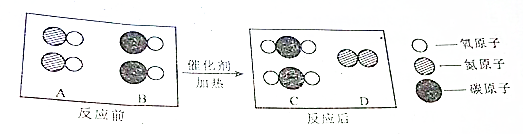
在变化前后,分子(填“原子”或“分子”,下同)发生了变化,原子的种类、数目没有改变;四种物质中,属于单质的是D(填标号);C物质中碳元素与氧元素的质量比为3:8.
分析 根据汽车尾气中有毒气体转化为无毒气体的微观示意图,结合化学变化的实质是分子分成原子,原子重新组合成新分子,由同种原子构成的分子为单质的分子,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:由汽车尾气中有毒气体转化为无毒气体的微观示意图,化学变化的实质是分子分成原子,原子重新组合成新分子,则在变化前后,分子发生了变化,原子的种类、数目没有改变.
由同种原子构成的分子为单质的分子,则四种物质中属于单质的是D.
C物质的1个分子由1个碳原子和2个氧原子构成,碳元素与氧元素的质量比为(12×1):(16×2)=3:8.
故答案为:分子;原子;D;3:8.
点评 本题通过微观粒子的反应模型图,考查化学变化的实质的认识,学会从微观的角度看物质、用微粒的变化分析物质的变化是正确解答此类题的关键.

练习册系列答案
相关题目
5.某温度时,A物质的溶解度是25g,则A的饱和溶液中溶质的质量分数是( )
| A. | 20% | B. | 25% | C. | 40% | D. | 50% |
2.下列关于二氧化碳性质的叙述错误的是( )
| A. | 二氧化碳能溶于水 | B. | 二氧化碳能使澄清的石灰水变浑浊 | ||
| C. | 二氧化碳用作人工降雨 | D. | 二氧化碳能与水发生反应生成碳酸 |
6.氢气还原氧化铜实验得到的固体粉末为氧化铜和铜的混合物.某化学兴趣小组的同学对该粉末中单质铜的含量进行测定;取10g粉末样品置于烧杯中,向其中分5此加入相同溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录如下:
实验所得数据见下表,请你分析并进行有关计算:
(1)表格中m=9.2;
(2)样品中单质铜的质量分数为71%;
(3)加入的稀硫酸溶质质量分数是多少?(写出计算过程)
实验所得数据见下表,请你分析并进行有关计算:
| 加入稀硫酸的质量(g) | 剩余固体质量(克) | |
| 第1次 | 10 | m |
| 第2次 | 10 | 8.4 |
| 第3次 | 10 | 7.6 |
| 第4次 | 10 | 7.1 |
| 第5次 | 10 | 7.1 |
(2)样品中单质铜的质量分数为71%;
(3)加入的稀硫酸溶质质量分数是多少?(写出计算过程)
17.某同学用一定溶质质量分数的稀硫酸做“氧化铜+硫酸→硫酸铜+水”的实验,其5次实验结果如表所示,根据实验结果填写下列空格:
(1)哪几次反应氧化铜有剩余?3、5
(2)表中x的值是16
(3)求硫酸溶液中溶质的质量分数.
| 实验次数 | 氧化铜/g | 硫酸溶液/g | 硫酸铜/g |
| 1 | 2.0 | 120 | 4.0 |
| 2 | 4.0 | 120 | 8.0 |
| 3 | 6.0 | 120 | 9.6 |
| 4 | 8.0 | 200 | 16 |
| 5 | 10.0 | 200 | X |
(2)表中x的值是16
(3)求硫酸溶液中溶质的质量分数.
