题目内容
化学学习小组的同学发现氢氧化钠与稀盐酸反应没有明显的现象.为了证明它们发生了反应,同学们从不同角度设计实验方案,并进行了实验.
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加稀盐酸,并不断振荡,同时测定混合溶液的pH,如果测定的pH逐渐变小且小于7,证明氢氧化钠与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是什么?
(2)简述强调要“测得溶液的pH小于7”的理由.
方案二:在氢氧化钠溶液中滴加几滴酚酞试液,溶液变红,再滴加稀盐酸到红色恰好变为无色.说明溶液中碱性消失,从而证明氢氧化钠与稀盐酸发生了反应.
该组同学实验时出现了意外情况:氢氧化钠中滴入酚酞变红后,过一会红色自动消失了.同学们猜想:
a、可能是酚酞与空气中氧气反应了; b、可能是氢氧化钠与空气中二氧化碳反应了.
(1)为验证猜想a,该组同学将氢氧化钠溶液加热,液面上方滴一些植物油,冷却后滴入酚酞试液,发现红色不会消失.“加热”和“滴植物油”目的是 .实验表明酚酞红色消失与空气中的氧气无关.
(2)关于猜想b,同学们分析认为氢氧化钠与二氧化碳反应生成碳酸钠,而碳酸钠溶液呈 性,
红色不会因此消失.
(3)同学们查阅资料得知:氢氧化钠溶液浓度过大时会出现上述意外现象.请你帮助他们设计实验证明他们使用的氢氧化钠溶液浓度过大.①实验方法
②观察到的现象 .
方案三:化学反应都伴随有能量变化,可借助反应中温度变化来判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10克混合,用温度计测定混合前后温度的变化值(△t),记录结果如下:
①3.65%盐酸、2.00%氢氧化钠溶液混合时,温度变化为3.5℃
②3.65%盐酸、4.00%氢氧化钠溶液混合时,温度变化为x℃
③7.30%盐酸、8.00%氢氧化钠溶液混合时,温度变化为14℃.
你认为第②次实验时,温度的变化结果应该是 ℃.
三组同学用各自不同的方法都证明了氢氧化钠溶液与稀盐酸之间能发生化学反应.他们给你留下了一道计算题,请你帮他们完成:
73克10%的稀盐酸中加入某种浓度的氢氧化钠溶液127克时,恰好完全反应.计算反应后所得溶液的溶质质量分数.
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加稀盐酸,并不断振荡,同时测定混合溶液的pH,如果测定的pH逐渐变小且小于7,证明氢氧化钠与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是什么?
(2)简述强调要“测得溶液的pH小于7”的理由.
方案二:在氢氧化钠溶液中滴加几滴酚酞试液,溶液变红,再滴加稀盐酸到红色恰好变为无色.说明溶液中碱性消失,从而证明氢氧化钠与稀盐酸发生了反应.
该组同学实验时出现了意外情况:氢氧化钠中滴入酚酞变红后,过一会红色自动消失了.同学们猜想:
a、可能是酚酞与空气中氧气反应了; b、可能是氢氧化钠与空气中二氧化碳反应了.
(1)为验证猜想a,该组同学将氢氧化钠溶液加热,液面上方滴一些植物油,冷却后滴入酚酞试液,发现红色不会消失.“加热”和“滴植物油”目的是
(2)关于猜想b,同学们分析认为氢氧化钠与二氧化碳反应生成碳酸钠,而碳酸钠溶液呈
红色不会因此消失.
(3)同学们查阅资料得知:氢氧化钠溶液浓度过大时会出现上述意外现象.请你帮助他们设计实验证明他们使用的氢氧化钠溶液浓度过大.①实验方法
②观察到的现象
方案三:化学反应都伴随有能量变化,可借助反应中温度变化来判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10克混合,用温度计测定混合前后温度的变化值(△t),记录结果如下:
①3.65%盐酸、2.00%氢氧化钠溶液混合时,温度变化为3.5℃
②3.65%盐酸、4.00%氢氧化钠溶液混合时,温度变化为x℃
③7.30%盐酸、8.00%氢氧化钠溶液混合时,温度变化为14℃.
你认为第②次实验时,温度的变化结果应该是
三组同学用各自不同的方法都证明了氢氧化钠溶液与稀盐酸之间能发生化学反应.他们给你留下了一道计算题,请你帮他们完成:
73克10%的稀盐酸中加入某种浓度的氢氧化钠溶液127克时,恰好完全反应.计算反应后所得溶液的溶质质量分数.
考点:中和反应及其应用,溶液的酸碱度测定,有关溶质质量分数的简单计算,碱的化学性质,根据化学反应方程式的计算
专题:常见的酸 酸的通性
分析:方案二:可以根据酚酞试液与其它物质相互作用时的现象等方面进行分析、考虑,从而得出正确的结论.例如,氢氧化钠溶液和空气中的二氧化碳反应生成碳酸钠,为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,就是为了验证是否是受二氧化碳的影响.
方案三:(1)由表中数据,可推出x的值.
(2)反应后所得溶液是氯化钠溶液,根据化学方程式NaOH+HCl=NaCl+H2O和盐酸中溶质的质量可以计算出生成氯化钠的质量,最后用氯化钠的质量除以所得溶液的质量乘以百分之百便可得反应后所得溶液中溶质的质量分数.
方案三:(1)由表中数据,可推出x的值.
(2)反应后所得溶液是氯化钠溶液,根据化学方程式NaOH+HCl=NaCl+H2O和盐酸中溶质的质量可以计算出生成氯化钠的质量,最后用氯化钠的质量除以所得溶液的质量乘以百分之百便可得反应后所得溶液中溶质的质量分数.
解答:解:方案二:(1)如果加热除去溶液中的少量氧气,再隔绝氧气,实验现象就不会受氧气影响了.
故填:赶走溶液中少量氧气,隔绝氧气.
(2)碱性溶液能使酚酞试液变红.
故填:碱
(3)①实验方法是:做对比实验,取上述NaOH溶液稀释,加入酚酞溶液;
②观察到的现象是:出现红色且不褪去.
故填:做对比实验,取上述NaOH溶液稀释,加入酚酞溶液;出现红色且不褪去.
方案三:(1)对比表中的数据可以知道:编号2中,氢氧化钠的质量分数是编号1的2倍,而3中氢氧化钠都是1的4倍,而温度变化也是4倍,所以编号2中温度变化应该编号1中温度的2倍,所以由表中数据,可推出x=7.故填:7;
(2)解:盐酸中HCl的质量为73g×10%=7.3g;
设反应生成的NaCl的质量为x.
NaOH+HCl=NaCl+H2O
36.5 58.5
7.3g x
=
x=11.7g
反应后所得溶液中溶质的质量分数为
×100%=5.85%
答:反应后所得溶液中溶质的质量分数为5.85%.
故填:赶走溶液中少量氧气,隔绝氧气.
(2)碱性溶液能使酚酞试液变红.
故填:碱
(3)①实验方法是:做对比实验,取上述NaOH溶液稀释,加入酚酞溶液;
②观察到的现象是:出现红色且不褪去.
故填:做对比实验,取上述NaOH溶液稀释,加入酚酞溶液;出现红色且不褪去.
方案三:(1)对比表中的数据可以知道:编号2中,氢氧化钠的质量分数是编号1的2倍,而3中氢氧化钠都是1的4倍,而温度变化也是4倍,所以编号2中温度变化应该编号1中温度的2倍,所以由表中数据,可推出x=7.故填:7;
(2)解:盐酸中HCl的质量为73g×10%=7.3g;
设反应生成的NaCl的质量为x.
NaOH+HCl=NaCl+H2O
36.5 58.5
7.3g x
| 36.5 |
| 7.3g |
| 58.5 |
| x |
x=11.7g
反应后所得溶液中溶质的质量分数为
| 11.7g |
| 73g+127g |
答:反应后所得溶液中溶质的质量分数为5.85%.
点评:本题主要考查了稀盐酸和氢氧化钠溶液发生中和反应及其设计实验进行相关方面证明等方面的内容,可以依据酸碱溶液的性质进行.还考查根据化学方程式计算和溶质质量分数的计算,难度不大.

练习册系列答案
相关题目
考虑到实验的安全、成功等问题,化学实验中常常需要特别关注实验的先后顺序.下列实验的先后顺序不正确的是( )
| A、点燃甲烷、氢气等可燃性气体之前,要先验纯,后点燃 |
| B、实验室制取气体时,要先检查装置的气密性,后加入试剂进行反应 |
| C、利用氯酸钾制氧气的实验结束时,要先把导气管从水槽中取出,后熄灭酒精灯 |
| D、用CO与氧化铁反应制取铁的实验结束时,要先停止通入CO,后停止加热固体 |
鉴别下列物质的方法不正确的是( )
| A、用水来鉴别氢氧化钠和硝酸铵 |
| B、用燃烧的方法鉴別腈纶毛线和纯羊毛毛线 |
| C、用燃烧的木条鉴别氧气和氮气 |
| D、用酚酞试液鉴别纯碱溶液和烧碱溶液 |
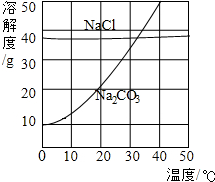 如图,为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线
如图,为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线 
