题目内容
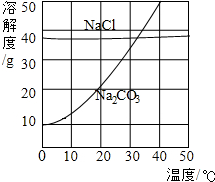 如图,为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线
如图,为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线 (1)生活在盐湖附近人们习惯“夏天晒盐,冬天捞碱”.请你解释:
(2)30℃时,欲配制等质量的氯化钠、碳酸钠两种物质的饱和溶液,所需水的质量关系是氯化钠
(3)将40℃的氯化钠、碳酸钠两种物质的饱和溶液各200g,降温至10℃,析出晶体的质量关系是氯化钠
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:根据题目信息和溶解度曲线可知:碳酸钠、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而氯化钠的溶解度受温度的影响较小;氯化钠的溶解度受温度的影响较小,适合于蒸发结晶的方法,因此夏天晒盐;碳酸钠的溶解度受温度的影响变化比较大,适合降温结晶的方法,因此冬天捞碱;30℃时,欲配制等质量的氯化钠、碳酸钠两种物质的饱和溶液,所需水的质量关系是氯化钠小于碳酸钠,因为在该温度下,氯化钠的溶解度比碳酸钠大;将40℃的氯化钠、碳酸钠两种物质的饱和溶液各200g,降温至10℃,析出晶体的质量关系是氯化钠小于碳酸钠,因为碳酸钠的溶解度受温度的影响变化比氯化钠大.
解答:解:(1)碳酸钠、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而氯化钠的溶解度受温度的影响较小;氯化钠的溶解度受温度的影响较小,适合于蒸发结晶的方法,因此夏天晒盐;碳酸钠的溶解度受温度的影响变化比较大,适合降温结晶的方法,因此冬天捞碱;故答案为:氯化钠的溶解度受温度的影响较小,适合于蒸发结晶的方法,因此夏天晒盐;碳酸钠的溶解度受温度的影响变化比较大,适合降温结晶的方法,因此冬天捞碱;
(2)30℃时,欲配制等质量的氯化钠、碳酸钠两种物质的饱和溶液,所需水的质量关系是氯化钠小于碳酸钠,因为在该温度下,氯化钠的溶解度比碳酸钠大;故答案为:<;
(3)将40℃的氯化钠、碳酸钠两种物质的饱和溶液各200g,降温至10℃,析出晶体的质量关系是氯化钠小于碳酸钠,因为碳酸钠的溶解度受温度的影响变化比氯化钠大;故答案为:<;
(2)30℃时,欲配制等质量的氯化钠、碳酸钠两种物质的饱和溶液,所需水的质量关系是氯化钠小于碳酸钠,因为在该温度下,氯化钠的溶解度比碳酸钠大;故答案为:<;
(3)将40℃的氯化钠、碳酸钠两种物质的饱和溶液各200g,降温至10℃,析出晶体的质量关系是氯化钠小于碳酸钠,因为碳酸钠的溶解度受温度的影响变化比氯化钠大;故答案为:<;
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
鱼油中富含的DHA(C22H32O2)是大脑细胞形成和发育不可缺少的物质.下列关于DHA的叙述中不正确的是( )
| A、DHA由三种元素组成 |
| B、DHA的相对分子质量为328 |
| C、DHA中碳、氢、氧元素的质量比是22:32:2 |
| D、DHA中氧元素的质量分数约是9.76% |
下列物质属于纯净物的是( )
| A、冰水混合物 | B、雪碧 |
| C、洁净的空气 | D、水泥砂浆 |
下列关于空气的叙述正确的是( )
| A、霓虹灯中常充入一种气体,通电时发出红光,该气体是氖气 |
| B、为了防止食品变质,常在包装中充入氧气 |
| C、氧气约占空气质量的五分之一,氮气约占空气质量的五分之四 |
| D、二氧化碳在空气中的含量增多会引起温室效应,属于空气污染物 |
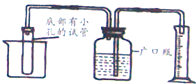 小王同学想对学校实验室中的锌铜合金中所含锌、铜的质量分数进行粗略测定.设计了如图所示的实验装置,选用了三种试剂:
小王同学想对学校实验室中的锌铜合金中所含锌、铜的质量分数进行粗略测定.设计了如图所示的实验装置,选用了三种试剂: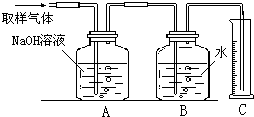
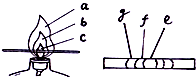 如图是探究酒精灯灯焰结构及性质的实验示意图:
如图是探究酒精灯灯焰结构及性质的实验示意图: