题目内容
课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3、还含有少量NaCl,其它杂质不计)和石灰乳(氢氧化钙的悬浊液)为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定.
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为: ;
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品.
【粗产品成分分析】
取适量粗产品溶于水,加入Ba(NO3)2溶液出现白色浑浊,该反应的化学方程式为 由此该粗产品中一定不含有 .
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为:
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品.
【粗产品成分分析】
取适量粗产品溶于水,加入Ba(NO3)2溶液出现白色浑浊,该反应的化学方程式为
考点:盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:(1)根据废碱液中的碳酸钠会与氢氧化钙反应进行分析;
【粗产品成分分析】(2)根据碳酸盐和氢氧化钙的性质来解答该题;
【粗产品成分分析】(2)根据碳酸盐和氢氧化钙的性质来解答该题;
解答:解:【粗产品制备】
(1)氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,
(2)【粗产品成分分析】
碳酸钠能和硝酸钡反应生成沉淀,化学方程式为:Na2CO3+Ba(NO3)2═BaCO3↓+2NaNO3,因为氢氧化钙和碳酸钠能反应,所以一定没有氢氧化钙.
答案:(1)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
【粗产品成分分析】(1)Ba(NO3)2+Na2CO3═BaCO3↓+2NaNO3;Ca(OH)2;
(1)氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,
(2)【粗产品成分分析】
碳酸钠能和硝酸钡反应生成沉淀,化学方程式为:Na2CO3+Ba(NO3)2═BaCO3↓+2NaNO3,因为氢氧化钙和碳酸钠能反应,所以一定没有氢氧化钙.
答案:(1)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
【粗产品成分分析】(1)Ba(NO3)2+Na2CO3═BaCO3↓+2NaNO3;Ca(OH)2;
点评:本题主要考查了化学方程式的书写、根据化学方程式计算、判断物质的组成等方面的问题.

练习册系列答案
相关题目
下列物质属于纯净物的是( )
| A、冰水混合物 | B、雪碧 |
| C、洁净的空气 | D、水泥砂浆 |
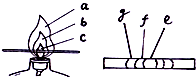 如图是探究酒精灯灯焰结构及性质的实验示意图:
如图是探究酒精灯灯焰结构及性质的实验示意图: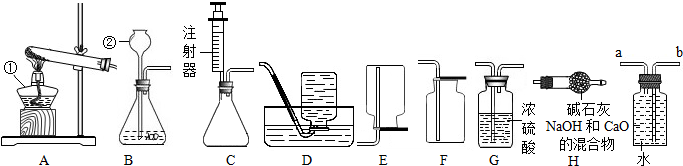
 某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进:
某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进: