题目内容
 做实验时,甲装置常用来制备气体,而乙装置有多项功能,可用来净化或收集气体.
做实验时,甲装置常用来制备气体,而乙装置有多项功能,可用来净化或收集气体.(1)若制备的气体是氢气,且产生的气体中不含酸性杂质气体,则试剂X常用
稀硫酸
稀硫酸
(填名称).当甲与乙相连(乙按图示放置)制备及收集氢气时,A应与C
C
(选填“B”或“C”)相连.(2)若X是稀盐酸、Y是石灰石,用甲、乙两种装置可组成发生、净化、收集
CO2
CO2
(填化学式)气体的系列装置.当乙作净化装置时,B
B
(选填“B”或“C”)与A相连,当乙中放入的是浓硫酸时,其目的是干燥气体或除去水蒸气
干燥气体或除去水蒸气
.(3)若X是水,Y是CaC2固体,则从A中放出乙炔(C2H2)气体,同时还生成一种碱.生成乙炔的化学方程式是
CaC2+2H2O=C2H2↑+Ca(OH)2
CaC2+2H2O=C2H2↑+Ca(OH)2
.乙炔微溶于水,密度与空气接近.若用装满水的乙装置收集乙炔时,A应与C
C
(选填“B”或“C”)相连.分析:(1)因为盐酸易挥发,硫酸不挥发,故用硫酸制取氢气;氢气的密度比水小;
(2)盐酸与石灰石反应可用来制取二氧化碳;当乙作净化装置,应长导管进气,了解浓硫酸的性质与应用;
(3)依据质量守恒定律推测碱是氢氧化钙,然后根据反应物、生成物书写方程式;根据气体的密度和溶水性确定收集装置;将两种情况都分析一下,看哪种情况合适.
(2)盐酸与石灰石反应可用来制取二氧化碳;当乙作净化装置,应长导管进气,了解浓硫酸的性质与应用;
(3)依据质量守恒定律推测碱是氢氧化钙,然后根据反应物、生成物书写方程式;根据气体的密度和溶水性确定收集装置;将两种情况都分析一下,看哪种情况合适.
解答:解:(1)因为盐酸易挥发,硫酸不挥发,故用硫酸制取氢气;因为氢气的密度很小,故A应与C连接;
(2)盐酸与石灰石反应可用来制取二氧化碳,所以甲、乙两种装置可组成发生、净化、收集二氧化碳;当乙作净化装置,应长导管进气,让气体与药品充分接触反应;而浓硫酸的作用为干燥气体或除去水蒸气;
(3)X是水,Y是CaC2固体,则从A中放出乙炔(C2H2)气体,同时还生成一种碱,依据质量守恒定律推测碱是氢氧化钙,反应的方程式是CaC2+2H2O=C2H2↑+Ca(OH)2;
乙炔微溶于水,若从B进,又会从C排出,若从C进,把水向下压,使水从B排出,可收集到乙炔;
故答案为:
(1)稀硫酸; C;
(2)CO2; B; 干燥气体或除去水蒸气;
(3)CaC2+2H2O=C2H2↑+Ca(OH)2; C.
(2)盐酸与石灰石反应可用来制取二氧化碳,所以甲、乙两种装置可组成发生、净化、收集二氧化碳;当乙作净化装置,应长导管进气,让气体与药品充分接触反应;而浓硫酸的作用为干燥气体或除去水蒸气;
(3)X是水,Y是CaC2固体,则从A中放出乙炔(C2H2)气体,同时还生成一种碱,依据质量守恒定律推测碱是氢氧化钙,反应的方程式是CaC2+2H2O=C2H2↑+Ca(OH)2;
乙炔微溶于水,若从B进,又会从C排出,若从C进,把水向下压,使水从B排出,可收集到乙炔;
故答案为:
(1)稀硫酸; C;
(2)CO2; B; 干燥气体或除去水蒸气;
(3)CaC2+2H2O=C2H2↑+Ca(OH)2; C.
点评:了解气体的干燥和净化;掌握二氧化碳、氢气的制取和收集方法;正确书写化学方程式,并会灵活应用知识解决问题.

练习册系列答案
相关题目
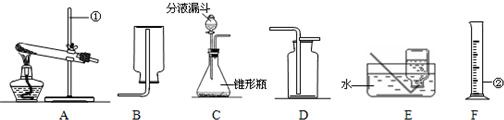

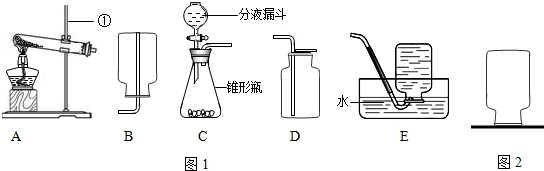
 做实验时,甲装置常用来制备气体,而乙装置有多项功能,可用来净化或收集气体.
做实验时,甲装置常用来制备气体,而乙装置有多项功能,可用来净化或收集气体.