题目内容
科学实验中要研究纯净物的组成、结构、性质等,常需要把混合物进行除杂、分离和提纯等.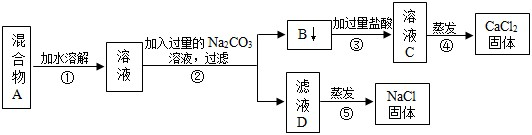
(1)除去二氧化碳气体中的水蒸气,可选用的试剂是 (写名称).
(2)除去N2中的O2,其方法是 (用化学方程式表示).
(3)为了将氯化钠和氯化钙两种固体混合物分离,设计了如图实验方案.
试回答下列问题:
①有的甲同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需增加一步实验,他的做法是 .
②为进一步探究混合物中氯化钠的质量分数,同学们分别提出了两个方案,方案1所选数据是称得混合物A的总质量还有沉淀B的质量;方案2所选数据是混合物A的总质量还有实验改进后所得的氯化钠固体的质量.判断哪个方案所选的数据不合理 .

(1)除去二氧化碳气体中的水蒸气,可选用的试剂是
(2)除去N2中的O2,其方法是
(3)为了将氯化钠和氯化钙两种固体混合物分离,设计了如图实验方案.
试回答下列问题:
①有的甲同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需增加一步实验,他的做法是
②为进一步探究混合物中氯化钠的质量分数,同学们分别提出了两个方案,方案1所选数据是称得混合物A的总质量还有沉淀B的质量;方案2所选数据是混合物A的总质量还有实验改进后所得的氯化钠固体的质量.判断哪个方案所选的数据不合理
考点:混合物的分离方法,常见气体的检验与除杂方法,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的分离和提纯
分析:(1)根据浓硫酸具有吸水性且不和二氧化碳反应进行分析;
(2)根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
(3)①由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,根据除杂的方法分析即可;
②方案2所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠.
(2)根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
(3)①由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,根据除杂的方法分析即可;
②方案2所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠.
解答:解:(1)浓硫酸具有吸水性且不和二氧化碳反应,因此除去二氧化碳气体中的水蒸气,可选用浓硫酸,故答案为:浓硫酸;
(2)氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:
2Cu+O2
2CuO.
(3)①由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠.根据除杂的条件可知,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,盐酸具有挥发性,所以蒸发后最后的固体物质是氯化钠,故答案为:向滤液D中加入足量的盐酸后再蒸发;
②方案1合理,称得沉淀B的质量,就可以根据化学反应方程式计算出混合物中氯化钙的质量,从而计算出氯化钠的质量,再称得混合物A的总质量,就可以根据质量分数公式计算出混合物中氯化钠的质量分数;方案2不合理,理由是所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠,故答案为:方案2不合理,理由是所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠.
故答案为:(1)浓硫酸;
(2)2Cu+O2
2CuO.
(3)①向滤液D中加入足量的盐酸后再蒸发;②方案2不合理,理由是所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠.
(2)氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:
2Cu+O2
| ||
(3)①由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠.根据除杂的条件可知,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,盐酸具有挥发性,所以蒸发后最后的固体物质是氯化钠,故答案为:向滤液D中加入足量的盐酸后再蒸发;
②方案1合理,称得沉淀B的质量,就可以根据化学反应方程式计算出混合物中氯化钙的质量,从而计算出氯化钠的质量,再称得混合物A的总质量,就可以根据质量分数公式计算出混合物中氯化钠的质量分数;方案2不合理,理由是所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠,故答案为:方案2不合理,理由是所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠.
故答案为:(1)浓硫酸;
(2)2Cu+O2
| ||
(3)①向滤液D中加入足量的盐酸后再蒸发;②方案2不合理,理由是所得氯化钠不仅包含原混合物中氯化钠,还包含实验过程中氯化钙与碳酸钠反应生成的氯化钠及过量的碳酸钠与稀盐酸生成的氯化钠.
点评:本题难度较大,掌握浓硫酸的性质、除锈的原理以及物质的转化等方面的知识是解决此类问题的关键.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、可以用pH试纸测定正常雨水的pH约为5.6 |
| B、可以用石蕊溶液来确定溶液的酸碱性 |
| C、医疗上可以用氯化钠来配制生理盐水 |
| D、工业上可以用硫酸生产化肥和农药 |
下列选项中属于化学变化的是( )
| A、冰雪消融 | B、石蜡熔化 |
| C、大米酿酒 | D、酒精挥发 |



