题目内容
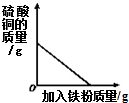
“药金”实为铜锌合金,它的外观与黄金相似,有些不法商贩用来冒充黄金谋取暴利.某同学为了研究“药金”的成分,取“药金”50g放入装有200g稀硫酸溶液的烧杯中,恰好完全反应.最后发现烧杯中物质的总质量比反应前(“药金”与稀硫酸溶液的总质量)减少了0.2g.
求:(1)药金中含锌多少克?
(2)药金中锌的质量分数是多少?
求:(1)药金中含锌多少克?
(2)药金中锌的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据质量守恒定律可以知道反应前后减少的质量即为生成氢气的质量,根据氢气的质量结合反应的化学方程式可以计算出锌的质量;
(2)根据锌和药金的质量代入质量分数计算公式,求药金中锌的质量分数.
(2)根据锌和药金的质量代入质量分数计算公式,求药金中锌的质量分数.
解答:解:(1)设铜锌合金中含有锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
=
解得:x=6.5g
(2)药金中锌的质量分数:
×100%=13%
答:药金中含锌6.5g,药金中锌的质量分数为13%.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
| 65 |
| 2 |
| x |
| 0.2g |
解得:x=6.5g
(2)药金中锌的质量分数:
| 6.5g |
| 50g |
答:药金中含锌6.5g,药金中锌的质量分数为13%.
点评:解答本题的关键是根据质量守恒定律得出氢气的质量,然后代入方程式计算即可.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
将一定量的乙醇(C2H6O)和氧气置于一个密闭的容器中引燃,测得反应前后各物质的质量如表所示( )
| 物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
| A、表中a的值为2.6 |
| B、X一定是该反应的催化剂 |
| C、X可能含有氢元素 |
| D、X一定含有碳元素 |
 课外小组同学利用如图所示装置进行实验.实验开始前红墨水左右两端液面保持相平,容器I、II体积相同,实验时将针筒内全部液体同时迅速注入容器中.实验内容如表所示.
课外小组同学利用如图所示装置进行实验.实验开始前红墨水左右两端液面保持相平,容器I、II体积相同,实验时将针筒内全部液体同时迅速注入容器中.实验内容如表所示.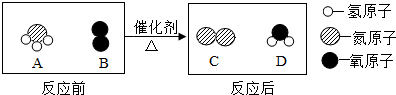
 的垃圾箱中的是
的垃圾箱中的是