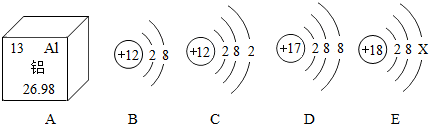题目内容
2.电解水时,常常要在水中加入少量硫酸钠以增强导电性,现将100g溶质质量分数为10%的硫酸钠溶液通电一段时间后,剩余溶液的质量为82g,试计算:(1)配制100g溶质质量分数为10%的硫酸钠溶液,需要硫酸钠10g;
(2)生成氢气和氧气的质量分别是多少克?
分析 (1)根据溶质质量=溶液质量×溶质质量分数解答;
(2)根据水的质量结合方程式计算生成氢气和氧气的质量.
解答 解:(1)配制100g溶质质量分数为10%的硫酸钠溶液,需要硫酸钠为100g×10%=10g;
(2)发生反应的水的质量为100g-82g=18g
设生成氧气的质量为x,生成的氢气的质量为y,
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,
36 4 32
18g y x
$\frac{36}{18g}$=$\frac{4}{y}$=$\frac{32}{x}$
解得:x=16g,y=2g
答:生成氢气2g;生成氧气16g.
点评 本题主要考查学生化学方程式进行计算和溶液计算的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
12.分类学习是学习化学的重要思想方法,下列各组物质的分类错误的是( )
| A. | 单质--铝 金刚石 氮气 | B. | 碱--烧碱 纯碱 熟石灰 | ||
| C. | 氧化物--氧化铜 二氧化锰 生石灰 | D. | 混合物--空气 粗盐 牛奶 |
13.下列物质的名称、俗名、化学式对应正确的是( )
| A. | 乙醇 酒精 C2H5OH | B. | 氧气 臭氧 O3 | ||
| C. | 氢氧化钠 烧碱 Na2CO3 | D. | 氢氧化钙 生石灰 Ca(OH)2 |
17.某兴趣小组发现了一包敞口放置的碱石灰样品,为探究其成分,同学们在实验室对这包碱石灰样品展开了探究.
【查阅资料】①碱石灰是由CaO和NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体.
②熟石灰微溶于水,且溶于水放出的热量很少可以忽略不计.
③BaCl2溶液显中性.
【提出猜想】根据资料,同学们分析碱石灰样品的主要成分可能含有CaO、NaOH、Ca(OH)2、CaCO3和碳酸钠.
【实验探究】小组讨论后设计如下实验进行探究:
【思考与分析】
小杰同学经过分析认为步骤②的结论不准确,原因是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【解释与结论】
通过以上探究与分析:可以得出该碱石灰样品一定含有的物质是Na2CO3、Ca(OH)2;实验探究步骤④所得溶液中除酚酞外还含有的溶质有NaOH、NaCl、BaCl2.
【查阅资料】①碱石灰是由CaO和NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体.
②熟石灰微溶于水,且溶于水放出的热量很少可以忽略不计.
③BaCl2溶液显中性.
【提出猜想】根据资料,同学们分析碱石灰样品的主要成分可能含有CaO、NaOH、Ca(OH)2、CaCO3和碳酸钠.
【实验探究】小组讨论后设计如下实验进行探究:
| 实验步骤及操作 | 实验现象 | 结论 |
| ①取部分该样品于试管中,加少量水 | 无明显放热现象 | 碱石灰样品中不含CaO和 氢氧化钠 |
| ②继续加足量水,振荡、静置 | 产生白色沉淀 | 样品中一定含有CaCO3 |
| ③从步骤②的试管中取少量上层清液于另一试管中,向其中滴加过量BaCl2溶液 | 产生白色沉淀 | / |
| ④将步骤③所得物质过滤,向滤液中滴加无色酚酞溶液 | 溶液变红色 |
小杰同学经过分析认为步骤②的结论不准确,原因是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【解释与结论】
通过以上探究与分析:可以得出该碱石灰样品一定含有的物质是Na2CO3、Ca(OH)2;实验探究步骤④所得溶液中除酚酞外还含有的溶质有NaOH、NaCl、BaCl2.
7.学习化学可以了解日常生活中某些变化的本质,下列变化中属于化学变化的是( )
| A. | 冰川融化 | B. | 葡萄酿酒 | C. | 西瓜榨汁 | D. | 玻璃破碎 |
11.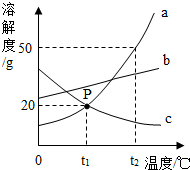 如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
 如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )| A. | t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c | |
| B. | P点表示t1℃时,a、c两种物质的溶解度相等 | |
| C. | 将c的饱和溶液变为不饱和溶液,可采用降温的方法 | |
| D. | t2℃时,将30g a物质加入到50g水中充分搅拌,得到80g a的饱和溶液 |
13.下表为氯化钠和氯化铵在不同温度时的溶解度,回答下列问题:
(1)由表中数据可知,溶解度随温度变化较大的物质是NH4Cl.
(2)20℃时100g水最多只能溶解NaCl36.0g,氯化钠与氯化铵溶解度相等的温度在10~20℃之间.
(3)向烧杯中加入100g水和50.0g氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体为12.8g.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(2)20℃时100g水最多只能溶解NaCl36.0g,氯化钠与氯化铵溶解度相等的温度在10~20℃之间.
(3)向烧杯中加入100g水和50.0g氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体为12.8g.
 某饮用水标签行的部分文字如图,请回答:
某饮用水标签行的部分文字如图,请回答: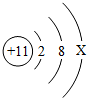 ,其中x=1.
,其中x=1.