题目内容
6.完成下列变化的化学方程式,并按要求填空:(1)高温煅烧石灰石:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;其基本反应类型是:分解反应.
(2)小苏打与稀盐酸反应:NaHCO3+HCl=NaCl+H2O+CO2↑;小苏打的用途有治疗胃酸过多.
(3)工业炼铁的主要原理是一氧化碳跟氧化铁在高温下反应:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)用氨水处理含硫酸的废水:2NH3•H2O+H2SO4═(NH4)2SO4+2H2O;反应的基本类型是:复分解反应.
(5)铁丝在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;集气瓶底部放少量水或细沙的目的是:防止降落的熔化物炸裂瓶底.
(6)用适量稀硫酸洗去铁钉的铁锈:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;溶液的颜色会变成黄色.
(7)实验室用高锰酸钾加热分解制氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;固体中锰元素的质量分数变化为变大(填“变大”或者“变小”或者“不变”).
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)碳酸钙在高温下生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;该反应符合“一变多”的特征,属于分解反应;
(2)小苏打与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑;可用于治疗胃酸过多;
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式
为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)氨水与硫酸反应生成硫酸铵和水,反应的化学方程式是2NH3•H2O+H2SO4═(NH4)2SO4+2H2O;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应;
(5)铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成黑色固体四氧化三铁,集气瓶底要放少量的水或细砂,目的是防止降落的熔化物炸裂瓶底.其化学反应方程式是:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(6)铁锈的主要成分是氧化铁,硫酸和氧化铁反应生成硫酸铁和水,故化学方程式为:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;溶液的颜色会变成黄色;
(7)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;由于反应后氧气逸出,完全反应后,固体混合物中锰元素的质量和原来相比变大.
故答案为:(1)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;分解反应;(2)NaHCO3+HCl=NaCl+H2O+CO2↑;治疗胃酸过多;(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(4)2NH3•H2O+H2SO4═(NH4)2SO4+2H2O;复分解反应;(5)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;防止降落的熔化物炸裂瓶底;(6)3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;黄色;
(7)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;变大
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

 科学实验活动册系列答案
科学实验活动册系列答案| A. | 置换反应生成单质和化合物,生成单质和化合物的反应一定是置换反应 | |
| B. | 单质中只含有一种元素,只含有一种元素的物质一定是单质 | |
| C. | 化合物是不同种元素组成的纯净物,不同种元素组成的纯净物一定是化合物 | |
| D. | 活泼金属能与稀酸反应放出气体,能与稀酸反应放出气体的一定是活泼金属 |
| A. | 用熟石灰鉴别氯化铵和氯化钾 | B. | 用食盐水制作叶脉书签 | ||
| C. | 用水鉴别硝酸铵和氯化钠 | D. | 用肥皂水鉴别硬水与软水 |
| A. | 碳酸钠 纯碱 Na2CO3 | B. | 氢氧化钙 石灰石 Ca(OH)2 | ||
| C. | 氧化钙 生石灰 CaO | D. | 氢氧化钠 火碱 NaOH |
| A. | 洗洁精能溶解油污 | |
| B. | 溶液上层的密度小,下层的密度大 | |
| C. | 固体、液体或气体都可以作为溶质 | |
| D. | 烧碱溶液和蔗糖溶液都具有很强的导电性 |
| A. | 黄铜 | B. | 铁矿石 | C. | 硬铝 | D. | 不锈钢 |
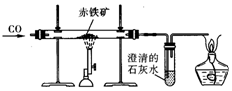 小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )
小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )(温馨提示:杂质不参加反应)
| A. | 玻璃管中的固体由黑色逐渐变成红色 | |
| B. | 剩余固体7.6g是得到的铁的质量 | |
| C. | 生成CO2的质量为2.4 g | |
| D. | 铁矿石样品中Fe2O3的质量分数为80% |
| A. | KNO3 | B. | NH4HCO3 | C. | KCl | D. | Ca(PO4)2 |