题目内容
2.在生活和化学实验中,人们经常用到各种除湿剂(干燥剂)(1)生石灰.白色块状固体,吸水后生成熟石灰,该反应的化学方程式为CaO+H2O═Ca(OH)2_.
(2)无水氧化钙.白色固体,有苦咸味,每千克吸水量为1kg~1.2kg,若1kg无水氯化钙吸收1.2kg水后得到氯化钙溶液,该溶液中溶质的质量分数为45.5%.
(3)浓硫酸.无色粘稠液体,有吸水性,在化学实验室常作干燥剂,但日常生活中却很少用它作除湿剂.其原因是浓硫酸具有强烈的腐蚀性(写出一点即可).
(4)还原铁粉.灰色或黑色粉末,又称“双吸剂”,能够吸收空气中的水分和氧气,常用于食品保鲜.检验使用一段时间后“双吸剂”是否仍有效的化学方法为取少量该“双吸剂”于试管中,滴加稀盐酸,若有气泡产生,则“双吸剂”还有效,否则无效.
分析 (1)生石灰与水反应生成氢氧化钙,写出反应的化学方程式即可.
(2)根据溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%,进行分析判断.
(3)根据浓硫酸具有强烈的腐蚀性,进行分析解答.
(4)铁粉能够吸收空气中的水分和氧气生成Fe2O3,结合铁与盐酸反应放出氢气,而Fe2O3与盐酸反应无气体生成,进行分析解答.
解答 解:(1)生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.
(2)若1kg无水氯化钙吸收1.2kg水后得到氯化钙溶液,该溶液中溶质的质量分数为$\frac{1kg}{1kg+1.2kg}×$100%≈45.5%.
(3)浓硫酸有吸水性,在化学实验室常作干燥剂,但日常生活中却很少用它作除湿剂,是因为浓硫酸具有强烈的腐蚀性.
(4)铁粉能够吸收空气中的水分和氧气生成Fe2O3,铁与盐酸反应放出氢气,而Fe2O3与盐酸反应无气体生成;因此检验使用一段时间后的“双吸剂”是否仍有效的化学方法为:取少量该“双吸剂”于试管中,滴加稀盐酸,若有气泡产生,则“双吸剂”还有效,否则无效.
故答案为:(1)CaO+H2O═Ca(OH)2;(2)45.5;(3)浓硫酸具有强烈的腐蚀性;(4)取少量该“双吸剂”于试管中,滴加稀盐酸,若有气泡产生,则“双吸剂”还有效,否则无效.
点评 本题难度不大,以各种除湿剂为素材考查了常见的干燥剂,掌握氧化钙的化学性质、溶质的质量分数、浓硫酸有吸水性、金属的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
12.某研究小组对CO2通入NaOH溶液,反应后所得溶液中的溶质成分进行探究.
查资料得知:CO2+2NaOH═Na2CO3+H2O(CO2少量或适量)
CO2+H2O+Na2CO3═2NaHCO3(CO2过量).
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
NaHCO3+NaOH═Na2CO3+H2O
Ca(HCO3)2可溶于水,Na2CO3受热不分解,
【定性分析】小虎同学认为溶质成分可能有三种情况,
1.NaOH和Na2CO3,原因是CO2不足(过量,不足,适量)
2.NaHCO3和Na2CO3
3.NaHCO3
小鹏同学认为还有一种情况是碳酸钠
小娥同学认为还有一种情况:NaHCO3和NaOH,你认为是否合理否(是或否)
小兰和小娟进行了以下实验并得出了结论,请完成表格:
【定量分析】根据小兰和小娟的结论,为确定该反应后混合物中Na2CO3的质量,小军进行了以下实验:
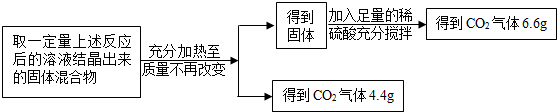
求所取固体混合物中Na2CO3的质量(写出计算过程)
查资料得知:CO2+2NaOH═Na2CO3+H2O(CO2少量或适量)
CO2+H2O+Na2CO3═2NaHCO3(CO2过量).
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
NaHCO3+NaOH═Na2CO3+H2O
Ca(HCO3)2可溶于水,Na2CO3受热不分解,
【定性分析】小虎同学认为溶质成分可能有三种情况,
1.NaOH和Na2CO3,原因是CO2不足(过量,不足,适量)
2.NaHCO3和Na2CO3
3.NaHCO3
小鹏同学认为还有一种情况是碳酸钠
小娥同学认为还有一种情况:NaHCO3和NaOH,你认为是否合理否(是或否)
小兰和小娟进行了以下实验并得出了结论,请完成表格:
| 现象 | 结论和解释 | |
| ①取上述反应后的溶液,加入足量的CaCl2溶液 | 有白色沉淀生成 | 原溶液中有Na2CO3(填写化学式,下同) 反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl |
| ②将①所得的浑浊液过滤,向滤液中加入足量的稀盐酸 | 产生大量气泡 | 原溶液中有Na2CO3 |
| ③另取②中的滤液,滴入几滴酚酞溶液, | 溶液由无色变成浅红色 | 滤液显碱性 |

求所取固体混合物中Na2CO3的质量(写出计算过程)
13.某电镀厂在对金属镀件表面除锈、除污过程中,使用了盐酸、硫酸、氢氧化钠、碳酸钠.该厂经处理后排放的废水含有H+、OH-、Na+、Fe3+、Cu2+、CO32-、Cl-、SO42-中的几种离子,某中学生环保志愿者小组对该废水中部分成分进行检测探究,实验步骤及现象如表所示.请你填写下表中每步实验现象所对应的实验结论.
根据以上信息综合分析,你推测该废水中除H2O外,还含有的物质是NaOH(写化学式,下同),可能存在的物质是NaCl、Na2SO4.
| 实验步骤及现象 | 实验结论(填离子符号) |
| 取废水样品观察,呈无色 | 废水中不含Fe3+、Cu2+ |
| 测所取废水样品的pH,pH=13 | 废水中含较多的OH- |
| 向废水样品中加入过量的稀盐酸,没有气泡产生 | 废水中不含CO32- |
10.表中除去物质所含杂质的方法正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CaCO3粉末 | KCl | 加水溶解、过滤、蒸发 |
| B | CO | CO2 | 通过灼热的Fe2O3 |
| C | NaCl溶液 | Na2CO3 | 加入适量稀盐酸 |
| D | H2 | HCl气体 | 通过NaOH溶液,再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
17.2011年3月22日是第十七届“世界水日”,主题是“城市用水:应对都市化挑战”.下列生活中常见的“水”属于纯净物的是( )
| A. | 矿泉水 | B. | 蒸馏水 | C. | 酸雨雨水 | D. | 生理盐水 |
7.厨房中几种物质在互相谈论着,你认为它们的叙述中属于物理变化的是( )
| A. |  玻璃杯:我被摔碎了 | B. |  煤气:我燃烧了 | ||
| C. |  菜刀:我生锈了 | D. |  食物:我腐烂了 |
11.物质的性质与用途密切关系.下列说法不正确的是( )
| A. | 铝的化学性质稳定,“银粉漆”( 铝粉)可涂在铁栏杆防锈 | |
| B. | 氧气能支持燃烧,可用作助燃剂 | |
| C. | 洗洁精具有乳化功能,可用于去油污 | |
| D. | 熟石灰呈碱性,可用于改良酸性土壤 |
16.在A+B=C+D的反应中,已知20g A和10g B恰好完全反应生成5g C,则5g A跟足量的B反应,生成D( )g.
| A. | 5 | B. | 10 | C. | 25 | D. | 6.25 |
