题目内容
4.下列有关金属的说法正确的是( )| A. | 纯金属和合金相比较,纯金属具有硬度大,抗腐蚀性好等优点 | |
| B. | 生铁和钢最主要的区别是含碳量不同,钢的含碳量比生铁要高,性能要优良 | |
| C. | 可以利用金属和氧气反应的难易和剧烈程度判断金属的化学活动性 | |
| D. | 铁生锈实际上是铁与氧气、水、二氧化碳等物质发生化学反应的过程 |
分析 A.根据纯金属和合金相比较,纯金属具有硬度比其合金小;
B.根据钢的含碳量比生铁要低;
C.根据金属和氧气反应的难易和剧烈程度与金属的化学活动性有关;
D.根据铁生锈实际上是铁与氧气、水等物质发生化学反应的过程;
解答 解:A.纯金属和合金相比较,纯金属具有硬度比其合金小; 错误;
B.钢的含碳量比生铁要低;错误;
C.金属和氧气反应的难易和剧烈程度与金属的化学活动性有关;可以利用金属和氧气反应的难易和剧烈程度判断金属的化学活动性,正确;
D.铁生锈实际上是铁与氧气、水等物质发生化学反应的过程;错误;
答案:C.
点评 了解常见金属的特性及合金的性质与分类,是解答此题的关键.

练习册系列答案
相关题目
14.“神舟七号”载人飞船实现了我国首次航天员出舱行走.运载火箭的发动机中使用了液氧,液氧的作用是( )
| A. | 支持燃料燃烧 | B. | 冷却发动机 | C. | 做燃料 | D. | 供给航天员呼吸 |
15.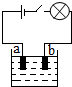 某同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如下表:
某同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如下表:
(1)由此实验可知,上述物质中属于非电解质的是蔗糖.
(2)进一步查阅资料可知,电解质能导电是由于在水溶液里或熔化状态下产生自由移动离子的结果.如氯化钠在水溶液里或熔化状态下能导电是产生了自由移动的Na+和Cl-的结果,其过程用电离方程式表示为NaCl=Na++Cl-.若上述实验时烧杯中所盛的是硫酸铜溶液,则闭合开关后,烧杯中的自由移动的离子由b向a方向移动的是Cl-.
(3)若上述实验中,向盛有硫酸铜溶液的烧杯中持续滴加氢氧化钡溶液,烧杯中发生反应的化学方程式为CuSO4+Ba(OH)2=Cu(OH)2↓+BaSO4↓,烧杯中的实验现象是生成蓝色和白色混合沉淀,预测将观察到灯泡的亮度变化情况是先变暗直至熄灭后逐渐变亮.
 某同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如下表:
某同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如下表:| 物质 导电性 状态 | 食盐NaCl | 硝酸钾KNO3 | 蔗糖C12H22O11 | 氢氧化钠NaOH | 硫酸铜CuSO4 |
| 固态 | × | × | × | × | × |
| 熔化状态 | √ | √ | × | √ | √ |
| 水溶液 | √ | √ | × | √ | √ |
(2)进一步查阅资料可知,电解质能导电是由于在水溶液里或熔化状态下产生自由移动离子的结果.如氯化钠在水溶液里或熔化状态下能导电是产生了自由移动的Na+和Cl-的结果,其过程用电离方程式表示为NaCl=Na++Cl-.若上述实验时烧杯中所盛的是硫酸铜溶液,则闭合开关后,烧杯中的自由移动的离子由b向a方向移动的是Cl-.
(3)若上述实验中,向盛有硫酸铜溶液的烧杯中持续滴加氢氧化钡溶液,烧杯中发生反应的化学方程式为CuSO4+Ba(OH)2=Cu(OH)2↓+BaSO4↓,烧杯中的实验现象是生成蓝色和白色混合沉淀,预测将观察到灯泡的亮度变化情况是先变暗直至熄灭后逐渐变亮.
12.下图为一组物质发生化学反应的示意图,其中 分别表示X、Y、R、Z四种不同元素的原子.右图分析,下了结论正确的是( )
分别表示X、Y、R、Z四种不同元素的原子.右图分析,下了结论正确的是( )

 分别表示X、Y、R、Z四种不同元素的原子.右图分析,下了结论正确的是( )
分别表示X、Y、R、Z四种不同元素的原子.右图分析,下了结论正确的是( )
| A. | 该反应属于置换反应 | |
| B. | “ ”表示的是化合物 ”表示的是化合物 | |
| C. | 该反应可表示为Y2+2Z2X$\frac{\underline{\;R\;}}{\;}$X2+2Z2 | |
| D. | R在该反应中的作用一定是加快反应速率 |
19.下列因素中能影响固体溶解度大小的是( )
| A. | 压强 | B. | 溶剂的质量 | C. | 搅拌 | D. | 温度 |
15.下列原子结构示意图中,属于非金属元素的是( )
| A. |  | B. |  | C. |  | D. |  |