题目内容
4.学好科学可以避免生活中的盲目行为.前段时间“吃碘防辐射”之说在社会上造成短暂的“盐荒”.如表是某地市场被抢购的一种“加碘食盐”包装袋上的部分说明.| 规格 | 250g/袋 |
| 配料 | 氯化钠碳酸钾 |
| 含碘量 | (20-30mg)/lKg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时同炖炒 |
| 贮藏方法 | 避先,避热、密封、防潮 |
(2)在救灾过程中,某些设备需要使用锂电池.锂电池中总的化学反应可表示成:Li+MnO2=LiMnO2该反应的反应基本类型是化合反应.
(3)配制该产品时每袋产品中最多加入碘酸钾12.6 毫克(计算结果保留一位小数).
分析 (1)根据在化合物中正负化合价代数和为零,进行解答.
(2)化合反应是指由两种或两种以上物质反应生成一种物质的反应;
(3)根据标签中含碘量(20-30mg)/1Kg及规格250g/袋,可求得该袋食盐中含碘元素的质量,然后由配料:氯化钠、碘酸钾(KIO3)可得知食盐中的碘元素都含有碘酸钾中,利用碘酸钾中碘元素的质量分数,可计算该袋食盐中所含碘酸钾的最大值
解答 解:(1)根据在化合物中正负化合价代数和为零,K元素的化合价为+1,氧元素的化合价为-2,可得碘酸钾中碘元素的化合价为:(+1)+x+(-2)×3=0,解得x=+5;
(2)由Li+MnO2=LiMnO2可知,反应物是两种,生成物是一种,属于化合反应.
(3)解:该袋加碘食盐中最多含碘元素的质量=250g÷1000×30mg/1Kg=7.5mg
配制该产品时每袋产品中最多加入碘酸钾的质量=7.5mg÷$\frac{127}{39+127+16×3}$×100%=12.6mg
故答案为:(1)+5(2)化合反应(3)12.6
点评 本题主要考查学生根据物质化学式分析,及对化合物中元素的质量分数计算方法的掌握与与在解题中应用能力.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
14.下列物质在氧气中燃烧火星四射的是( )
| A. | 硫 | B. | 铁 | C. | 镁 | D. | 碳 |
15.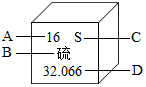 图是元素周期表中硫元素的信息示意图,对图中信息理解正确的是( )
图是元素周期表中硫元素的信息示意图,对图中信息理解正确的是( )
 图是元素周期表中硫元素的信息示意图,对图中信息理解正确的是( )
图是元素周期表中硫元素的信息示意图,对图中信息理解正确的是( )| A. | 原子序数 | B. | 元素符号 | C. | 元素名称 | D. | 原子质量 |
1.推理是一种重要的学习方法,下列推理正确的是( )
| A. | 分子可以构成物质,则物质一定是由分子构成的 | |
| B. | 离子是带电的原子或原子团,则带电的粒子都是离子 | |
| C. | 碱能使酚酞试液变红,则能使酚酞试液变红的物质一定是碱 | |
| D. | 单质是由同种元素组成的,则同种元素组成的纯净物一定是单质 |



