题目内容
16.科学家此采用“组合转化”技术,可将二氧化碳在一定条件下转化为重要的化工原料乙烯,其反应的微观过程如图所示,下列说法不正确到是( )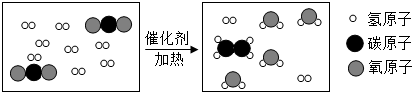
| A. | 参加反应的两种分子的个数比是1:4 | |
| B. | 反应前后分子的数目减少了 | |
| C. | 反应前后原子种类,数目均不变 | |
| D. | 乙烯的化学式为C2H4 |
分析 观察反应的微观过程图,分析反应物、生成物,写出反应的化学方程式,据其意义分析判断有关的问题.
解答 解:由反应的微观过程图可知,各物质反应的微粒个数关系是:
据微观示意图可知:CO2和H2在条件下转化为化工原料乙烯(C2H4)和水,配平即可,故其化学方程式为:2CO2+6H2$\frac{\underline{催化剂}}{△}$C2H4+4H2O,因此:
A、由方程式可知,参加反应的两种分子的个数比是2:6=1:3,故说法不正确;
B、由方程式可知,每8个分子变化成5个分子,反应前后分子的数目减少了,故说法正确;
C、根据质量守恒定律及微观示意图,可知反应前后原子种类、数目均不变,故说法正确D;
D、由微粒的构成可知,乙烯的化学式为C2H4,故说法正确.
故选项为:A.
点评 本题考查学生的识图能力,通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
4.如图所示,对实验内容的分析不正确的是( )

| A. | 甲:弹簧弯曲,说明力可以改变物体的形状 | |
| B. | 乙:乒乓球不掉落,说明气体压强与气体流速有关 | |
| C. | 丙:①试管中铁钉生锈,说明铁生锈需要与空气(或氧气)和水接触 | |
| D. | 丁:烧杯中溶液变为无色,说明盐酸与氢氧化钠发生了反应 |
11.在设计测定空气中氧气含量的实验时,如下说法不合理的是( )
| A. | 在一般情况下,要选择密闭的装置,最好有比较准确的体积刻度 | |
| B. | 实验前,要检查装置的气密性 | |
| C. | 实验结束后,要恢复到室温,再读数 | |
| D. | 铜粉、木炭、红磷都是可以选择的药品 |
1.工业上利用在高温的条件下煅烧石灰石(主要成分为CaCO3)的方法生产石灰(主要成分为CaO),同时得到CO2,该反应的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
据此填写如表:
据此填写如表:
| 反应物 | 生成物 | ||
| CaCO3 | CaO | CO2 | |
| 质量比 | 100 | 56 | 44 |
| A | 50g | 28g | 22g |
5.下列说法正确的是( )
| A. | 金属都能导电,所以能导电的单质一定是金属 | |
| B. | 经测定只含磷元素的物质,一定不可能是合金 | |
| C. | 金属单质的硬度一定比非金属单质的硬度大 | |
| D. | 常温下金属都是固态的,非金属全部是气态或固态的 |
6.要配制100g溶质质量分数0.9%的氯化钠溶液,需氯化钠的质量是( )
| A. | 0.9 克 | B. | 9克 | C. | 99.1克 | D. | 100克 |

