题目内容
1.工业上利用在高温的条件下煅烧石灰石(主要成分为CaCO3)的方法生产石灰(主要成分为CaO),同时得到CO2,该反应的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.据此填写如表:
| 反应物 | 生成物 | ||
| CaCO3 | CaO | CO2 | |
| 质量比 | 100 | 56 | 44 |
| A | 50g | 28g | 22g |
分析 根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,以及质量守恒定律、物质的相对分子质量进行分析.
解答 解:碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
| 反应物 | 生成物 | ||
| CaCO3 | CaO | CO2 | |
| 质量比 | 100 | 56 | 44 |
| A | 50g | 28g | 22g |
| 反应物 | 生成物 | ||
| CaCO3 | CaO | CO2 | |
| 质量比 | 100 | 56 | |
| A | 50g | 22g | |
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.

练习册系列答案
相关题目
16.科学家此采用“组合转化”技术,可将二氧化碳在一定条件下转化为重要的化工原料乙烯,其反应的微观过程如图所示,下列说法不正确到是( )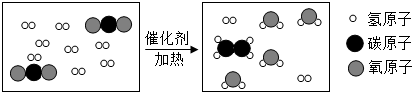

| A. | 参加反应的两种分子的个数比是1:4 | |
| B. | 反应前后分子的数目减少了 | |
| C. | 反应前后原子种类,数目均不变 | |
| D. | 乙烯的化学式为C2H4 |
6.下列物质中能与稀硫酸发生反应,又能产生无色气体的是( )
| A. | Ba(OH)2 | B. | K2CO3 | C. | Mg(OH)2 | D. | BaCl2 |
13. 如图是实验室里一瓶标签破损的白色粉末状固体,小明同学取出少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明溶液,继续滴加稀盐酸,有无色无味的气体产生,该固体可能是( )
如图是实验室里一瓶标签破损的白色粉末状固体,小明同学取出少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明溶液,继续滴加稀盐酸,有无色无味的气体产生,该固体可能是( )
 如图是实验室里一瓶标签破损的白色粉末状固体,小明同学取出少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明溶液,继续滴加稀盐酸,有无色无味的气体产生,该固体可能是( )
如图是实验室里一瓶标签破损的白色粉末状固体,小明同学取出少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明溶液,继续滴加稀盐酸,有无色无味的气体产生,该固体可能是( )| A. | Na2SO4 | B. | NaCl | C. | Na2CO3 | D. | NaOH |
10.随着生活节奏的加快,方便的小包装食品越来越受到人们的欢迎.为了防止富脂食品氧化变质和受潮,生产厂家往往在食品包装袋中放入装有某些化学物质的小袋.你认为放在这些小袋中的物质可能是( )
| A. | 蔗糖、无水硫酸铜 | B. | 食盐、生石灰 | C. | 铁粉、生石灰 | D. | 烧碱、熟石灰 |
11.下列实验现象中,描述正确的是( )
| A. | 木炭在氧气中燃烧,有无色刺激性气味气体生成 | |
| B. | 红磷在氧气中剧烈燃烧,有黄色火焰,有大量白色气体生成 | |
| C. | 纯净的氢气在空气中安静的燃烧,产生淡蓝色的火焰,在火焰上方罩一个干冷小烧杯,烧杯内壁有水雾出现 | |
| D. | 铁丝在氧气中剧烈燃烧,放出大量的热,火星四射,有黑色熔融物溅落瓶底 |