题目内容
9.小科在探究CO2和NaOH是否发生反应时,设计出下列三种装置进行实验: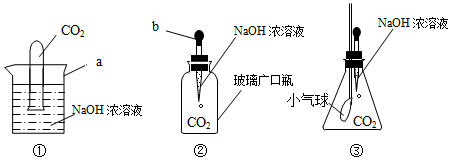
(1)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:实验①试管内液面上升.
(2)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广口瓶,以使实验取得成功,你将选用的物品是矿泉水瓶(或塑料瓶等),改进后能看到的实验现象是矿泉水瓶变瘪.
(3)如果有同学质疑,认为上述实验设计没有排除CO2可能溶解于NaOH溶液的假设,你如何进一步设计实验证明CO2和NaOH肯定发生了化学反应?①将水槽中的氢氧化钠溶液换成水与实验①做对比实验.从对比实验中可以看出,液体换成水后,试管中液面上升的幅度较小,在氢氧化钠溶液中,试管中液面上升的幅度较大.
②取少量反应后的溶液于试管中,滴加氯化钙溶液,如果溶液变浑浊,表明二氧化碳与氢氧化钠反应了.
③取少量反应后的溶液于试管中,滴入稀盐酸,如果出现气泡,则说明CO2确实同NaOH发生了化学反应,生成了碳酸钠.
分析 (1)二氧化碳能和氢氧化钠溶液反应生成碳酸钠和水,①中的二氧化碳和氢氧化钠溶液反应后,试管内的压强减小,从而使液体在试管内逐渐上升.而③中塑料瓶可以用作检验二氧化碳能和氢氧化钠溶液反应的容器,因为塑料瓶可以随着压强的变化而膨胀或收缩,可以据此完成解答.
(2)塑料瓶可以用作检验二氧化碳能和氢氧化钠溶液反应的容器,因为塑料瓶可以随着压强的变化而膨胀或收缩.
(3)可以设计对照实验或根据二氧化碳和氢氧化钠溶液反应生成了碳酸钠,解答该题.
解答 解:(1)实验①中试管中的二氧化碳气体和烧杯中的浓氢氧化钠溶液反应后,试管内压强减小,所以试管内液面会逐渐上升,形成水柱;
(2)可以用塑料瓶代替玻璃广口瓶,这样实验现象就明显了,因为二氧化碳被氢氧化钠溶液吸收后,瓶内压强减小,在外界大气压的作用下,塑料瓶变瘪.
(3)①将水槽中的氢氧化钠溶液换成水与实验①做对比实验.从对比实验中可以看出,液体换成水后,试管中液面上升的幅度较小,在氢氧化钠溶液中,试管中液面上升的幅度较大.
②取少量反应后的溶液于试管中,滴加氯化钙溶液,如果溶液变浑浊,则表明二氧化碳与氢氧化钠反应了,化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl.
③取少量反应后的溶液于试管中,滴入稀盐酸,如果出现气泡,则说明CO2确实同NaOH发生了化学反应,生成了碳酸钠,化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:(1)试管内液面上升;
(2)矿泉水瓶(或塑料瓶等);矿泉水瓶变瘪;
(3)①将水槽中的氢氧化钠溶液换成水与实验①做对比实验.从对比实验中可以看出,液体换成水后,试管中液面上升的幅度较小,在氢氧化钠溶液中,试管中液面上升的幅度较大.
②取少量反应后的溶液于试管中,滴加氯化钙溶液,如果溶液变浑浊,表明二氧化碳与氢氧化钠反应了.
③取少量反应后的溶液于试管中,滴入稀盐酸,如果出现气泡,则说明CO2确实同NaOH发生了化学反应,生成了碳酸钠.(合理即可)
点评 本题主要考查氢氧化钠和二氧化碳的性质,利用不同实验设计进行现象的分析和评价,并能进行实验改进.

| A. | 氢氧化铁 | B. | 硫酸铜 | C. | 水 | D. | 硝酸 |
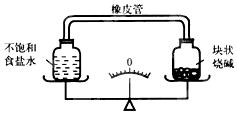
| A. | 指针偏左,食盐溶液一定变浓,烧碱变质 | |
| B. | 指针偏右,食盐溶液一定饱和,烧碱潮解 | |
| C. | 指针偏左,食盐溶液一定变浓,烧碱潮解 | |
| D. | 指针偏右,食盐溶液一定变浓,烧碱潮解 |
| 溶液 | 盐酸 | CuCl2溶液 | Na2SO4溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
| pH | <7 | <7 | =7 | =7 | >7 | >7 |
| A. | 盐溶液可能显酸性、碱性或中性 | B. | pH>7一定是碱的溶液 | ||
| C. | pH=7一定是盐溶液 | D. | pH<7可能是碱溶液 |
| A. | 1:8 | B. | 2:1 | C. | 4:5 | D. | 9:10 |
| A. | 氧气、硫酸、碳酸钙、冰水混合物 | B. | 氢气、盐酸、硫酸钠、硫酸铜晶体 | ||
| C. | 铜、硝酸、食盐、空气 | D. | 金刚石、醋酸、熟石灰、石油 |