题目内容
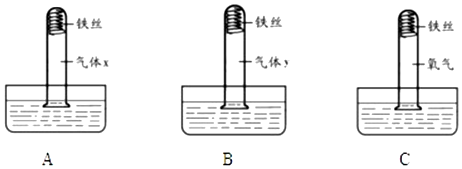
19.如图是实验室用于制取、干燥和收集气体的装置图.科学实验课上同学们用锌和稀硫酸反应制取并收集氢气,请回答问题: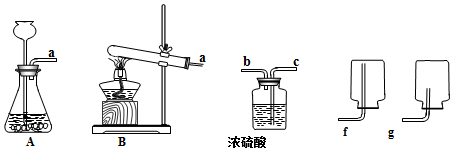
(1)制取氢气实验的发生装置应选择(填装置编号)A.
(2)现要收集一瓶干燥的氢气,请在上述装置中选择合适的装置,按气体的流向用导管的编号将装置连接好:a→c→b→f.
分析 (1)回忆氢气的反应装置和反应原理:制取氢气使用固体+液体反应,不需加热,根据反应原理,选取发生装置;
(2)根据干燥气体的方法以及氢气的密度来分析.
解答 解:(1)在实验室中,常用锌粒与稀硫酸反应来制取氢气,属于固液常温型,所以选择装置A来制取;故填:A;
(2)要除去氢气中的水蒸气可以通过盛有浓硫酸的洗气瓶,氢气从长管进入,短管排出,因为氢气的密度比空气小,所以用向下排空气法来收集,为了将集气瓶中的空气排净,导管要伸入集气瓶的底部,故填:c→b→f.
点评 气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
14.某校科学兴趣小组的同学对五个品牌味精(A、B、C、D、E)中NaCl的含量进行测定.下面是该小组所做的实验步骤:
①称取某种品牌味精样品m克放入烧杯中,加适量蒸馏水完全溶解.
②加入足量稀硝酸和硝酸银溶液(待填).
③过滤,用蒸馏水洗涤沉淀2-3次.
④将沉淀烘干、称量,测得固体质量为m1克.
⑤实验数据记录.
(1)补齐实验步骤②加入足量稀硝酸和硝酸银溶液
(2)求D品牌味精中NaCl的质量分数.
| 味精品牌 | A | B | C | D | E |
| 样品质量m(克) | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 |
| 沉淀质量m1(克) | 4.7 | 4.8 | 4.8 | 4.9 | 5.2 |
②加入足量稀硝酸和硝酸银溶液(待填).
③过滤,用蒸馏水洗涤沉淀2-3次.
④将沉淀烘干、称量,测得固体质量为m1克.
⑤实验数据记录.
(1)补齐实验步骤②加入足量稀硝酸和硝酸银溶液
(2)求D品牌味精中NaCl的质量分数.
4.实验室一般不用块状石灰石与硫酸反应制取二氧化碳,原因是碳酸钙与硫酸反应生成的硫酸钙微溶,覆盖在石灰石的表面阻止与硫酸接触继续反应.小明思考能否加入某种物质使其反应继续进行,他查阅资料后发现,在石灰石与硫酸反应停止后,加入少量氯化钠固体,能观察到在较长的时间内一直保持较快且平稳反应并产生气体.
小明又思考新的问题,加氯化钠后,石灰石能与硫酸较快地发生反应,在反应中起促进作用是Na+、还是Cl-,还是二者共同作用的结果呢?然后设计了如下实验:向5支试管里各加入一块石灰石和5mL浓度为50%的硫酸,待反应停止后,再分别加入约0.2克的KCl、NH4Cl、CaCl2、…等固体轻轻振荡.观察到的现象记录于如表:
(1)石灰石与硫酸反应停止后,加入氯化钠固体反应继续进行,其原因可能是氯化钠能够增大硫酸钙在溶液中的溶解度,或氯化钠能使硫酸钙在石灰石表面脱落,或氯化钠能够破坏碳酸钙表面的硫酸钙等;
(2)小明为了验证Na+在实验中的作用,在上表①处应加入的物质是硝酸钠;
(3)通过实验可得出的结论是加快石灰石与硫酸反应是Na+与Cl-共同起作用,Cl-所起的用比Na+大,钙离子对该反应起抑制作用.
小明又思考新的问题,加氯化钠后,石灰石能与硫酸较快地发生反应,在反应中起促进作用是Na+、还是Cl-,还是二者共同作用的结果呢?然后设计了如下实验:向5支试管里各加入一块石灰石和5mL浓度为50%的硫酸,待反应停止后,再分别加入约0.2克的KCl、NH4Cl、CaCl2、…等固体轻轻振荡.观察到的现象记录于如表:
| 物质 | KCl | NH4Cl | CaCl2 | ① |
| 现象 | 继续发生反应生成二氧化碳气体,但反应较慢,反应一段时间后就趋于停止. | CaCl2溶解并生成大量的白色固体,但不能继续发生反应 | 没有明显 可见的现象 | |
(2)小明为了验证Na+在实验中的作用,在上表①处应加入的物质是硝酸钠;
(3)通过实验可得出的结论是加快石灰石与硫酸反应是Na+与Cl-共同起作用,Cl-所起的用比Na+大,钙离子对该反应起抑制作用.
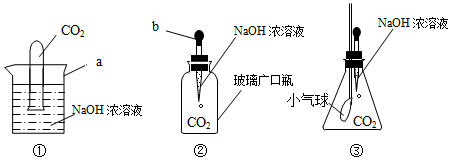

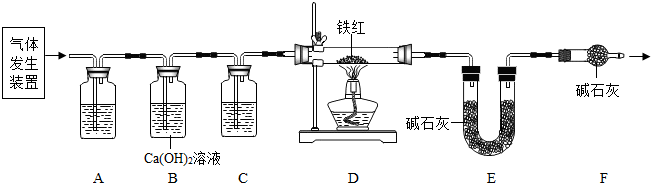
 小李用图1气体发生装置来制取二氧化碳,老师给他提供了石灰石、稀盐酸.小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图2所示,最后还有少量石灰石剩余.(不计水蒸发和稀盐酸的挥发且2HCl+CaCO3═CaCl2+H2O+CO2↑)
小李用图1气体发生装置来制取二氧化碳,老师给他提供了石灰石、稀盐酸.小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图2所示,最后还有少量石灰石剩余.(不计水蒸发和稀盐酸的挥发且2HCl+CaCO3═CaCl2+H2O+CO2↑)