题目内容
某固体样品含一定质量的碳酸钙和22.2g氯化钙,此固体样品与一定量的稀盐酸恰好完全反应,所得溶液的质量为 100.8g,测得溶液中钙元素的质量为12g.试计算:
(1)反应后所得溶液中溶质的质量.
(2)稀盐酸中溶质的质量分数.
(1)反应后所得溶液中溶质的质量.
(2)稀盐酸中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)固体样品中的碳酸钙与稀盐酸恰好完全反应,使得反应后溶液为变成氯化钙溶液;根据溶液中钙元素的质量,利用氯化钙中钙元素质量分数,计算溶质氯化钙的质量;
(2)根据题意,计算稀盐酸中溶质的质量分数,需要解决稀盐酸的质量及其中溶质HCl的质量,溶质HCl的质量可根据化学方程式,由碳酸钙的质量计算求得;而稀盐酸的质量需要利用质量守恒定律进行计算.
(2)根据题意,计算稀盐酸中溶质的质量分数,需要解决稀盐酸的质量及其中溶质HCl的质量,溶质HCl的质量可根据化学方程式,由碳酸钙的质量计算求得;而稀盐酸的质量需要利用质量守恒定律进行计算.
解答:解:
(1)反应后所得溶液中溶质氯化钙的质量=12g÷
×100%=33.3g
(2)设样品中碳酸钙的质量为x,反应消耗HCl的质量为y,生成二氧化碳的质量为z.
反应生成氯化钙的质量=33.3g-22.2g=11.1g
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
x y 11.1g z
=
=
=
x=10g
y=7.3g
z=4.4g
稀盐酸中溶质的质量分数=
×100%=10%
答案:(1)反应后所得溶液中溶质的质量是33.3g;(2)稀盐酸中溶质的质量分数为10%.
(1)反应后所得溶液中溶质氯化钙的质量=12g÷
| 40 |
| 111 |
(2)设样品中碳酸钙的质量为x,反应消耗HCl的质量为y,生成二氧化碳的质量为z.
反应生成氯化钙的质量=33.3g-22.2g=11.1g
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
x y 11.1g z
| 100 |
| x |
| 73 |
| y |
| 111 |
| 11.1g |
| 44 |
| z |
x=10g
y=7.3g
z=4.4g
稀盐酸中溶质的质量分数=
| 7.3g |
| 100.8g+4.4g-(10g+22.2g) |
答案:(1)反应后所得溶液中溶质的质量是33.3g;(2)稀盐酸中溶质的质量分数为10%.
点评:根据化学方程式能表示反应中各物质的质量比,由反应中某物质的质量可以计算反应中其它物质的质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
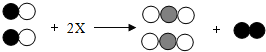
如图为氧化汞受热分解时的微观过程示意图,由此得出的下列信息不正确的是( )

| A、反应前后,原子的数目不变 |
| B、该反应过程中,原子发生了重新组合 |
| C、反应过程中,原子是最小的粒子 |
| D、反应前后,分子的种类不变 |
下列对相关实验现象的描述错误的是( )
| A、木炭在氧气中燃烧发出白光 |
| B、把铁钉放入硫酸铜溶液中,铁钉的表面有铜生成 |
| C、硫在空气中燃烧发出淡蓝色火焰 |
| D、红磷在空气中燃烧产生大量白烟 |
2014年诺贝尔化学奖授予贝齐格、莫纳和黑尔三位科学家,得奖者的研究允许人类从单一分子的角度观察病毒以至细胞内的蛋白质,对了解有关物质的功能、结构作出重大贡献.下列有关说法错误的是( )
| A、该成果提升了光学显微镜的分辨率 |
| B、分子是由原子构成的,分子大原子小 |
| C、人类已能够利用并操控分子的运动 |
| D、该研究为人类探索病毒世界提供了新途径 |
 向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答:
向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答:
 .
.