题目内容
13.某同学向足量的石灰石中加入105.4g稀盐酸,充分反应后过滤,得到含氯化钙10%的溶液1llg,则稀盐酸中氢元素的质量分数为( )| A. | 5.1% | B. | 10.5% | C. | 15.7% | D. | 20.3% |
分析 稀盐酸中氢元素的质量分数=$\frac{HCl中氢元素质量+水中氢元素质量}{稀盐酸质量}$×100%,因此需要根据反应化学方程式,由反应生成的氯化钙的质量计算出稀盐酸中溶质HCl的质量,然后分别计算出溶质、溶剂中所含H元素质量.
解答 解:设稀盐酸中HCl的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 111
x 111g×10%
$\frac{73}{111}=\frac{x}{111g×10%}$
x=7.3g
则稀盐酸中氢元素的质量分数:$\frac{7.3g×\frac{1}{36.5}+(105.4g-7.3g)×\frac{2}{18}}{105.4g}$×100%=10.5%
故选B.
点评 解答本题时需要引起注意的是:所求稀盐酸中氢元素的质量分数,水和氯化氢中都含有氢元素,不能只考虑氯化氢中的氢元素.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列各组物质,按单质、氧化物、混合物顺序排列的是( )
| A. | 石墨、碳酸钙、石油 | B. | 铜、氧化镁、自来水 | ||
| C. | 臭氧、二氧化硫、冰水混合物 | D. | 水、干冰、空气 |
8.下列相关事实用微观粒子的知识解释错误的是 ( )
| 事 实 | 解 释 | |
| A | 湿衣服晾干 | 水分子不断运动 |
| B | 蔗糖溶液不导电 | 蔗糖溶液中没有自由移动的带电粒子 |
| C | 盐酸、稀硫酸具有相似化学性质 | 都含有相同的氢元素 |
| D | 热胀冷缩 | 粒子之间的间隔受热增大,遇冷减小 |
| A. | A | B. | B | C. | C | D. | D |
9.关于下列的说法正确的是( )
| A. | 分子由原子构成,所以分子比原子大 | |
| B. | 原子中的原子核一定含有中子 | |
| C. | 原子的最外层电子数跟该原子对应的元素的化学性质关系密切 | |
| D. | 中子和质子是最小的粒子 |
10.当前,世界已经迈向了“低碳”时代,选择“低碳”既是一种生活方式也是一种生存责任.公交系统推广使用节能减排的双燃料公交车,这种公交车以天然气为主要燃料.下图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图.
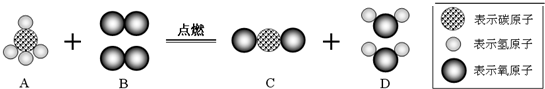
请根据示意图回答下列问题:
(1)用微粒观点分析,上述反应前后原子种类和数目一定不变.
(2)写出上述反应的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
则a的值为2.8,根据表格中数据,请完成相关的化学方程式4CH4+7O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2CO+8H2O.

请根据示意图回答下列问题:
(1)用微粒观点分析,上述反应前后原子种类和数目一定不变.
(2)写出上述反应的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
| 物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |




