题目内容
某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质).取样品10.0g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如下图所示.(有关反应:NaHCO3+HCl=NaCl+H2O+CO2↑)
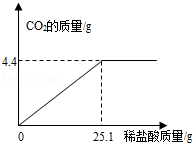
求:(1)样品中碳酸氢钠的质量分数.
(2)恰好完全反应时,所得溶液中溶质的质量分数.
【答案】
84%;24.3%
【解析】
试题分析:设样品中碳酸氢钠的质量为x,生成氯化钠的质量为y
NaHCO3+HCl=NaCl+H2O+CO2↑
84 58.5 44
x y 4.4g
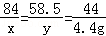
x=8.4g
y=5.85g
样品中碳酸氢钠的质量分数=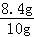 ×100%=84%
×100%=84%
恰好完全反应时,所得溶液中溶质的质量分数=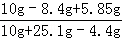 ×100%=24.3%
×100%=24.3%
答:(1)样品中碳酸氢钠的质量分数约为84%;
(2)恰好完全反应时,所得溶液中溶质的质量分数为24.3%
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
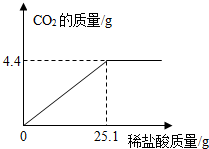 (2013?普宁市模拟)某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质).取样品10.0g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如图所示.(有关反应:NaHCO3+HCl=NaCl+X+CO2↑)求:
(2013?普宁市模拟)某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质).取样品10.0g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如图所示.(有关反应:NaHCO3+HCl=NaCl+X+CO2↑)求: 碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.
碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.
