题目内容
1.我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法.(1)实验室制取气体时,确定发生装置需要考虑的两种因素有AC(填序号).
A.反应物的状态 B.气体的密度
C.反应的条件 D.气体的溶解性
(2)某实验室的仪器柜里有如下仪器:

其中仪器④的名称是锥形瓶.
(3)老师提出用碳酸钠粉末与稀盐酸制取二氧化碳,其反应的化学方程式为2HCl+Na2CO3═2NaCl+H2O+CO2↑.为了完成该实验,有四位同学组装了以下发生装置,你认为最不合适的一套装置是A(填字母序号),理由是用碳酸钠粉末与稀盐酸制取二氧化碳,不需加热,常温进行.写出该装置可以制取另外一种气体的化学反应方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.

(4)要产生22g二氧化碳气体,至少需要碳酸钠粉末的质量是53g.
(5)二氧化碳也是一种宝贵的资源.固定和利用二氧化碳的一个成功范例是:在高温高压下二氧化碳和氨气(NH3)可以合成尿素[CO(NH2)2],同时生成水.该反应的化学方程式为CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O.
分析 (1)实验室制取气体时,确定发生装置需要考虑反应物的状态、反应的条件;
(2)据常用仪器的认识分析;
(3)根据碳酸钠粉末与稀盐酸反应生成氯化钠和水和二氧化碳,不需加热,常温进行解答;
(4)利用产生二氧化碳的质量,根据反应的化学方程式,计算出样品中碳酸钠的质量;
(5)根据反应写出反应的化学方程式;
解答 解:(1)实验室制取气体时,确定发生装置需要考虑反应物的状态、反应的条件;故填:AC;
(2)仪器④的名称是锥形瓶;
(3)用碳酸钠粉末与稀盐酸制取二氧化碳,不需加热,常温进行;最不合适的一套装置是A;A装置需要加热,可以用高锰酸钾制氧气,也可以用氯酸钾制氧气,如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)设碳酸钠的质量为x.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 22g
$\frac{106}{x}=\frac{44}{22g}$
x=53g
(5)高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水.该反应的化学方程式为:CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O.
答案:
(1)AC;
(2)锥形瓶;
(3)A;用碳酸钠粉末与稀盐酸制取二氧化碳,不需加热,常温进行;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)53;
(5)CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和检查装置的气密性等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 干冰能升华 | B. | 氮气是一种无色无味的气体 | ||
| C. | 浓盐酸易挥发 | D. | 氢氧化钠在空气中易变质 |
| A. | O2 | B. | 2O | C. | 2O2 | D. | O2- |
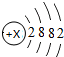 探究元素周期表可寻得一些规律.如图是一些元素的原子结构示意图.例:碳原子结构示意图的意思:6C表示6号元素碳,
探究元素周期表可寻得一些规律.如图是一些元素的原子结构示意图.例:碳原子结构示意图的意思:6C表示6号元素碳,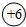 表示核内带6个单位正电荷,
表示核内带6个单位正电荷,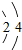 表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.
表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.