题目内容
8.“低碳”是全世界的主题,以下流程是通过控制化学反应的条件来促进或抑制化学反应,实现“低碳”,从而更好地通过化学反应为人类造福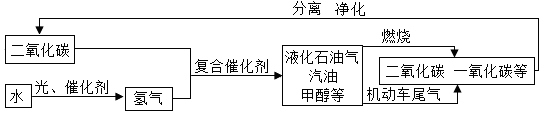
根据上述流程回答下列问题:(1)上述流程中可循环利用的物质是二氧化碳.
(2)除去机动车尾气中一氧化碳,下列方法中不正确的是bc.
a.把混合气体通过灼热的氧化铜b.把混合气体点燃c.把混合气体倾倒到另一个容器中
(3)甲醇(CH3OH)燃烧除了生成二氧化碳外,还生成一种常温下为液态的化合物,写出反应的化学方程式2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O,如何证明燃烧产物中含有二氧化碳,你设计的实验方法是Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
分析 (1)根据工艺流程可以判断上述流程中可循环利用的物质;
(2)高温条件下,氧化铜和一氧化碳反应生成铜和二氧化碳;
二氧化碳不能燃烧,不支持燃烧;
(3)甲醇燃烧生成水和二氧化碳,二氧化碳能使澄清石灰水变浑浊.
解答 解:(1)上述流程中可循环利用的物质是二氧化碳.
故填:二氧化碳.
(2)a.把混合气体通过灼热的氧化铜时,一氧化碳和氧化铜反应生成铜和二氧化碳,该选项可以除去一氧化碳;
b.二氧化碳不支持燃烧,因此不能把混合气体点燃,该选项不能除去一氧化碳;
c.把混合气体倾倒到另一个容器中时,不能除去一氧化碳,该选项不能除去一氧化碳.
故填:bc.
(3)甲醇燃烧的化学方程式为:2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O;
证明燃烧产物中含有二氧化碳的实验方法是:把燃烧产物通入澄清石灰水中,澄清石灰水变浑浊,说明产物中含有二氧化碳,二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:2CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O;Ca(OH)2+CO2═CaCO3↓+H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
19.某同学用下表对所学的部分物质进行分类,其中错误的是( )
| 选项 | 物质分类依据 | 同一类物质举例 |
| A | 混合物 | 空气、钢、氯化钠溶液 |
| B | 碳单质 | 金刚石、石墨、C60 |
| C | 常见的碱 | 火碱、纯碱、熟石灰 |
| D | 有机物 | 甲烷、酒精、葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |
16.某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应).请计算:
(1)上表中n的数值为2.8.
(2)样品中碳酸钙的质量分数是82.5%.
(3)求盐酸中溶质的质量分数.
NaOH含量的测定:
同学取10.0g含氢氧化钠(碳酸钠)粗产品,逐滴加入20%的盐酸至恰好完全反应时,消耗盐酸的质量为36.5g.放出CO2 0.44g(不考虑二氧化碳气体的溶解).求原粗产品中NaOH质量分数.(写出计算过程)
| 序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 第1次 | 20 | 11 |
| 第2次 | 20 | 6 |
| 第3次 | 20 | 2.8 |
| 第4次 | 20 | n |
(2)样品中碳酸钙的质量分数是82.5%.
(3)求盐酸中溶质的质量分数.
NaOH含量的测定:
同学取10.0g含氢氧化钠(碳酸钠)粗产品,逐滴加入20%的盐酸至恰好完全反应时,消耗盐酸的质量为36.5g.放出CO2 0.44g(不考虑二氧化碳气体的溶解).求原粗产品中NaOH质量分数.(写出计算过程)
3.FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验.实验小组同学通过查阅资料,进行了尝试.

不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.右表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
(1)实验中,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式CuO+2HCl═CuCl2+H2O;你认为步骤b调节溶液的pH到3.2~4.7(填数值范围)比较合适.
(2)实验中,步骤d加稀盐酸前,因缺少洗涤(填操作名称)而使获得的氯化铁溶液不纯.
(3)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用C(用字母表示)最合理.
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.

不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.右表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
(2)实验中,步骤d加稀盐酸前,因缺少洗涤(填操作名称)而使获得的氯化铁溶液不纯.
(3)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用C(用字母表示)最合理.
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.
