题目内容
1.小鹏与小明做完酸、碱、盐相关性质实验后,很感兴趣地把稀硫酸、氢氧化钠溶液和碳酸钠溶液混合在一起,看到有大量气泡生成.他们对反应后溶液中溶质的成分很是好奇,请你与他们一起进行探究.【提出问题】反应后溶液中溶质的成分是什么?
【猜想假设】猜想①:Na2SO4、Na2CO3;猜想②:Na2SO4、Na2CO3、NaOH;猜想③:Na2SO4、H2SO4、
Na2CO3;猜想④:Na2SO4、H2SO4;猜想⑤:Na2SO4.
上述猜想中,你认为不合理的是猜想③(填序号).
【实验探究】(1)小鹏取少量该溶液于试管中,向其中滴加无色酚酞试液,发现溶液颜色不变.据此,他认为猜想⑤是正确的.你认为他的结论是不合理(填“合理”或“不合理”)的,理由是酚酞试液遇中性和酸性溶液均不变色.
(2)小明向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝.该反应的化学方程式是CuO+H2SO4═CuSO4+H2O.
【实验结论】根据上述实验探究,你认为猜想④(填序号)是正确的.
【拓展应用】
(1)工厂与实验室的酸性废水必须处理至中性再排放,这样做的意义是以免腐蚀下水道钢管(答一点即可).
(2)在分析化学反应后所得物质成分时,除考虑生成物外还要考虑反应物是否过量.
分析 【猜想假设】
根据碳酸钠和硫酸能反应,不能共存解答;
【实验探究】
(1)根据硫酸钠溶液和硫酸溶液,不能使无色酚酞变色解答;
(2)稀硫酸的溶液显酸性,能和氧化铜反应,溶液变蓝,说明溶液中有硫酸并写出化学方程式;
【实验结论】碳酸钠的溶液显碱性,稀硫酸的溶液显酸性,滴加无色酚酞,发现溶液颜色无变化,排除①②,向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝,排除⑤;
【拓展应用】根据酸碱反应解答;根据实验的结论进行发生反思.
解答 解:
【猜想假设】
稀硫酸、氢氧化钠溶液和碳酸钠溶液混合一起反应时,如果稀硫酸滴加过快,稀硫酸和碳酸钠反应,开始也会产生气泡,有二氧化碳生成,有可能没把氢氧化钠消耗完,稀硫酸已经没有了,故②合理;碳酸钠和硫酸能反应,不能共存,故③不合理;
【实验探究】
(1)取少量该溶液于试管中,向其中滴加无色酚酞,发现溶液颜色无变化,说明溶液中无碳酸钠和氢氧化钠,故④⑤都符合,因此小鹏的结论是不合理,理由是④Na2SO4、H2SO4也不能使无色酚酞变色;
(2)向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝.说明溶液中有硫酸,反应的化学方程式为:CuO+H2SO4═CuSO4+H2O;
【实验结论】碳酸钠的溶液显碱性,稀硫酸的溶液显酸性,滴加无色酚酞,发现溶液颜色无变化,排除①②,向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝,排除⑤;故④是正确的;
【拓展应用】实验室的酸性废水必须处理至中性再排放可以减少水的污染.因为反应可能是完全反应,也可能是其中的一种反应物过量,因此在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量;
故答案:
【猜想假设】③
【实验探究】
(1)不合理;酚酞试液遇中性和酸性溶液均不变色(合理即可);
(2)CuO+H2SO4═CuSO4+H2O
【实验结论】④
【拓展应用】(1)以免腐蚀下水道钢管(或染污环境) (2)反应物是否过量.
点评 本题主要考查化学实验方案的设计与评价,根据物质的性质和物质间的反应规律,学会运用猜想与事实验证的方法和技巧处理实验问题

 口算题天天练系列答案
口算题天天练系列答案| A. | 该制造过程属于化学变化 | |
| B. | 钯催化剂能催化所有的反应 | |
| C. | “钯催化交叉偶联反应”有利于人类合成复杂分子 | |
| D. | 利用该技术能改变合成途径,降低反应发生的条件 |
【提出问题】该固体的成分是什么?
【查阅资料】①Cu是紫红色固体 ②Cu2O是红色固体 ③Cu2O+H2SO4(稀)=CuSO4+Cu+H2O
【猜想与假设】
猜想一:Cu 猜想二:Cu、Cu2O 猜想三:Cu、C 猜想四:Cu、Cu2O、C
小晨同学认为猜想一不正确,因为反应后的固体不完全是紫红色.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取少量固体置于烧杯中,加入足量稀硫酸,观察溶液颜色 | 溶液呈蓝色 | 猜想三不正确 |
| 步骤二:把步骤一中所得混合物过滤,将滤渣干燥后置于滤纸上,观察固体颜色 | 固体为紫红色、黑色 | 猜想四正确 |
【拓展延伸】下列可以用于鉴别真、假黄金的方法是BCD(填字母).
A.观察颜色 B.加热固体 C.滴加稀硫酸 D.滴加硝酸银溶液.
| A. | Na | B. | H | C. | N2 | D. | H2O |
| A. | 水银-Ag | B. | 两个氢原子:2H | C. | 镁离子:Mg+2 | D. | 干冰-H2O |
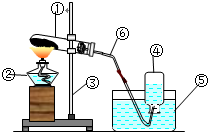 如图是实验室用加热高锰酸钾的方法制取氧气的装置图
如图是实验室用加热高锰酸钾的方法制取氧气的装置图