题目内容
14.X、Y两金属都能与AgNO3溶液反应,置换出Ag;X跟H2SO4不反应,Y跟H2SO4反应生成H2,由此判断X、Y可能依次是( )| A. | Fe,Hg | B. | Fe,Zn | C. | Cu,Hg | D. | Cu,Zn |
分析 根据题意,X、Y两金属都能与AgNO3溶液反应,置换出Ag,说明X、Y两金属的活动性均比银强;X跟H2SO4不反应,Y跟H2SO4反应生成H2,说明X的金属活动性比氢弱,Y的金属活动性比氢强;即Y>H>X>Ag,据此进行分析判断.
解答 解:X、Y两金属都能与AgNO3溶液反应,置换出Ag,说明X、Y两金属的活动性均比银强;X跟H2SO4不反应,Y跟H2SO4反应生成H2,说明X的金属活动性比氢弱,Y的金属活动性比氢强;即Y>H>X>Ag.
A、铁排在氢的前面,不符合H>X,故选项错误.
B、铁排在氢的前面,不符合H>X,故选项错误.
C、铜排在氢的后面,汞排在氢的后面,不符合Y>H>X,故选项错误.
D、铜排在氢的后面,锌排在氢的前面,符合Y>H>X>Ag,故选项正确.
故选:D.
点评 本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.某同学对酸碱盐的知识进行了以下梳理
(1)请根据下表盐中的金属元素的排列顺序,填写空格中的化学式:
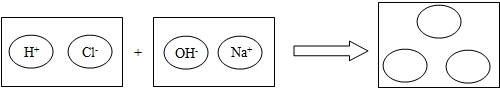
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在如图的圆圈中填入适当的化学式或离子符号应该是H2O,Na+,Cl-.
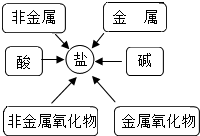
(3)此同学通过查阅资料,发现许多反应都有盐类物质生成(如图).比如①用稀硫酸除铁锈;②古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,①、②中任选一个,写出反应的化学方程式:Fe+CuSO4═FeSO4+Cu(或Fe2O3+3H2SO4═Fe2(SO4)3+3H2O).
(1)请根据下表盐中的金属元素的排列顺序,填写空格中的化学式:
| KNO3 | Ca(NO3)2 | Na(NO3)2 | Mg(NO3)2 | Al(NO3)3 | Zn(NO3)2 | Fe(NO3)2 |

(3)此同学通过查阅资料,发现许多反应都有盐类物质生成(如图).比如①用稀硫酸除铁锈;②古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,①、②中任选一个,写出反应的化学方程式:Fe+CuSO4═FeSO4+Cu(或Fe2O3+3H2SO4═Fe2(SO4)3+3H2O).

2.2013年3月底,上海、安徽等地出现H7N9新型流感病毒,严重威胁了人们的健康,其治疗的有效药物达菲,可以用莽草酸(C7H10O5)制取.下列有关莽草酸的说法正确的是( )
| A. | 莽草酸中氢元素的质量分数最大 | B. | 莽草酸由碳、氢、氧三种元素组成 | ||
| C. | 莽草酸中各元素的质量比为7:10:5 | D. | 每个莽草酸分子里含有5个氢分子 |
6.为验证A、B、C三种金属的活动性,将它们分别投入稀盐酸中,只有C不能与盐酸作用产生气体.再把A投入B的硝酸盐溶液中,在A的表面有B析出.则三种金属的活动性顺序为( )
| A. | B>A>C | B. | A>B>C | C. | B>C>A | D. | C>A>B |
6.早晚空腹喝牛奶,不如喝牛奶时吃一些馒头等食品,后者利用价值高,原因是前者被人体吸收的氨基酸主要被用于( )
| A. | 氧化分解 | B. | 合成新的自身蛋白质 | ||
| C. | 合成脂肪 | D. | 以上三者都不是 |


