题目内容
5.现有混合气体由SO3、SO2、O2中的两种物质组成,则该混合气体中,硫元素的质量分数不可能是( )| A. | 40% | B. | 45% | C. | 30% | D. | 70% |
分析 由化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,分别计算出SO2、SO3、O2中硫元素的质量分数,进而判断出混合气体中硫元素的质量分数的范围,进行分析解答.
解答 解:SO2中硫元素的质量分数为$\frac{32}{32+16×2}$×100%=50%;SO3中硫元素的质量分数为$\frac{32}{32+16×3}$×100%=40%,O2中硫元素的质量分数为0;则SO2中硫元素的质量分数最高,它不论和其它哪一种或者2种混合,硫元素的质量分数都小于50%,由此可知不论怎么混合都不可能出现混合气体中硫元素的质量分数等于或高于50%的情况,即硫元素的质量分数应在0~50%之间.
故选:D.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
9.下列常见水果中呈碱性的是( )
| A. |  柠檬pH=1.5 | B. |  苹果pH=4.1 | C. |  菠萝pH=5.1 | D. |  柿子pH=8.5 |
16.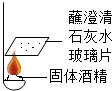 在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:
在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:
【查阅资料】(1)该“固体酒精”是用酒精、氯化钙和氢氧化钠按一定比例混合而成的;
(2)氯化钙、氯化钡溶液显中性.
【提出问题】(1)酒精中是否含有碳元素;(2)氢氧化钠是否变质.
【实验探究】
(1)按如图实验,发现澄清石灰水变浑浊,说明固体酒精中含碳元素(填“含”或“不含”).
(2)取少量“固体酒精”放在烧杯中,加足量的水充分搅拌后,静置,发现烧杯底部有白色沉淀,取沉淀于试管中,加稀盐酸,产生气泡.写出生成气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.分析实验可知氢氧化钠已经(填“已经”或“没有”)变质.
(3)为了进一步确定氢氧化钠变质的程度,分组探究:
①甲组烧杯中的上层溶液放在两支试管中,按如图探究:
②乙组同学认为甲组实验不能证明清液中一定含有氢氧化钠,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.他们另取烧杯中的上层清液,加足量的氯化钡溶液,充分反应后滴加酚酞溶液,溶液变红.
【实验结论】“固体酒精”中氢氧化钠部分变质.
【反思交流】乙组实验加入足量氯化钡溶液的目的是使碳酸钠完全反应.
【拓展应用】要除去部分变质的氢氧化钠中杂质,可选用适量的AC(填字母).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
 在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:
在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:【查阅资料】(1)该“固体酒精”是用酒精、氯化钙和氢氧化钠按一定比例混合而成的;
(2)氯化钙、氯化钡溶液显中性.
【提出问题】(1)酒精中是否含有碳元素;(2)氢氧化钠是否变质.
【实验探究】
(1)按如图实验,发现澄清石灰水变浑浊,说明固体酒精中含碳元素(填“含”或“不含”).
(2)取少量“固体酒精”放在烧杯中,加足量的水充分搅拌后,静置,发现烧杯底部有白色沉淀,取沉淀于试管中,加稀盐酸,产生气泡.写出生成气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.分析实验可知氢氧化钠已经(填“已经”或“没有”)变质.
(3)为了进一步确定氢氧化钠变质的程度,分组探究:
①甲组烧杯中的上层溶液放在两支试管中,按如图探究:
| 方案 | 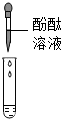 | 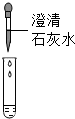 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 溶液中有氢氧化钠 | 溶液中由碳酸钠 |
【实验结论】“固体酒精”中氢氧化钠部分变质.
【反思交流】乙组实验加入足量氯化钡溶液的目的是使碳酸钠完全反应.
【拓展应用】要除去部分变质的氢氧化钠中杂质,可选用适量的AC(填字母).
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
13.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下(说明:一种小球代表一种原子).则下列说法不正确的是( )


| A. | 反应前后原子的种类发生改变 | |
| B. | 图示中共有4种分子 | |
| C. | 该图示说明在化学变化中分子可分,原子不可分 | |
| D. | 以上反应符合质量守恒定律 |
10.下列物质中,属于纯净物的是( )
| A. | 洁净的空气 | B. | 盐酸溶液 | C. | 冰水混合物 | D. | 泥沙 |
17.类推是化学学习中常用的思维方法,现有以下类推结果,其中正确的是( )
| A. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性 | |
| C. | 氧化物都含有氧元素,所以含氧元素的化合物一定是氧化物 | |
| D. | 活泼金属能与稀硫酸反应放出气体,所以能与稀硫酸反应放出气体的物质一定是活泼金属 |
14.下列反应属于分解反应的是( )
| A. | Ca(HCO3)2$\stackrel{加热}{→}$CaCO3+CO2+H2O | B. | Mg+H2SO4→MgSO4+H2 | ||
| C. | Fe+O2$\stackrel{点燃}{→}$Fe3O4 | D. | C2H5OH+O2$\stackrel{点燃}{→}$CO2+H2O |

 A、B是不含结晶水的两种固体物质,溶解度曲线如图所示,请回答下列问题:
A、B是不含结晶水的两种固体物质,溶解度曲线如图所示,请回答下列问题: