题目内容
10. 据报道,某硫酸化工厂周边河流出现大量鱼类死亡事件.环保局技术员小于和小芳马上对河流水质进行检测.
据报道,某硫酸化工厂周边河流出现大量鱼类死亡事件.环保局技术员小于和小芳马上对河流水质进行检测.(1)小芳首先用PH检测仪测出河水的pH<7,说明水质呈酸性.在实验室,我们也可以用PH试纸来简单检测河水的酸碱度,简述操作的主要步骤:用玻璃棒蘸取河水样品滴在pH试纸上,把试纸呈现的颜色与标准比色卡对照.
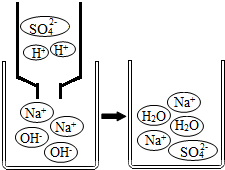
(2)小于采集了硫酸厂排放的污水样品,在实验室通过氢氧化钠溶液中和滴定酸的方法,以确定污水中硫酸的浓度.右图为氢氧化钠溶液和硫酸溶液反应前后的微观示意图,请根据如图从微观角度说明中和反应的实质是酸碱溶液中氢离子和氢氧根离子反应生成水.
(3)经滴定检测该污水中含0.98%的硫酸.为除去污染,技术员小于建议厂方用熟石灰中和污水后再排放.现若中和100吨该污水,需用熟石灰多少吨?(已知:反应化学方程式为 Ca(OH)2+H2SO4═CaSO4+2H2O)
分析 (1)根据用pH试纸测定溶液的酸碱度的正确方法分析解答.
(2)根据图示分析从微观角度说明中和反应的实质;
(3)根据硫酸雨氢氧化钙反应的方程式,由硫酸的质量求出氢氧化该的质量.
解答 解:(1)可用PH试纸来简单检测河水的酸碱度,操作的主要步骤是:用玻璃棒蘸取河水样品滴在pH试纸上,把试纸呈现的颜色与标准比色卡对照;
(2)由微粒的变化可知,酸碱溶液中氢离子和氢氧根离子反应生成水;
(3)设需要熟石灰的质量为x
H2SO4 +Ca(OH)2=CaSO4+2H2O
98 74
100t×0.98% x
$\frac{98}{74}=\frac{100t×0.98%}{x}$
x=0.74t
答:(1)用玻璃棒蘸取河水样品滴在pH试纸上,把试纸呈现的颜色与标准比色卡对照;(2)酸碱溶液中氢离子和氢氧根离子反应生成水;(3)需要熟石灰的质量为0.74t.
点评 主要考查学生对中和反应的认识,以及运用化学方程式和溶质质量分数公式进行计算的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
1.如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )


| A. | 该反应是稀HCl滴入NaOH溶液中 | |
| B. | ag是指加入氢氧化钠固体质量 | |
| C. | A点溶液的溶质为HCl和NaCl | |
| D. | 检验B点溶液的溶质先滴加足量的AgNO3,静置后再滴入少量Ba(NO3)2 |
18.《舌尖上的中国》第二季介绍了很多中国的美食及其制作方法.下列关于“饮食健康”说法正确的是( )
| A. | 用甲醛浸泡海产品 | |
| B. | 用地沟油烹饪食物 | |
| C. | 用工业酒精来勾兑饮用酒 | |
| D. | 在煲好的鸡汤中放入适当的加碘食盐 |
2.正确的实验操作对实验结果、人身安全都非常重要,下列实验操作正确的是( )
| A. |  滴加液体 | B. |  稀释浓硫酸 | ||
| C. |  移走蒸发皿 | D. |  检验装置的气密性 |
19.如图食物中富含维生素的是( )
| A. |  肥肉 | B. |  山芋 | C. |  青椒 | D. |  鸡蛋 |
 A~H和X都是初中化学中常见物质,其中A、D是无色气体,B、E是红色固体,F为白色沉淀,H为红褐色沉淀,它们的转化关系如图所示.
A~H和X都是初中化学中常见物质,其中A、D是无色气体,B、E是红色固体,F为白色沉淀,H为红褐色沉淀,它们的转化关系如图所示.