题目内容
7. 下面关于水电解实验的叙述不正确的是( )
下面关于水电解实验的叙述不正确的是( )| A. | 实验说明水是由氢、氧两种元素组成的 | |
| B. | 此实验为了增强水的导电性,常常往水中加入稀硫酸 | |
| C. | 水电解的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| D. | 若a试管气体为10g,则b试管气体为5g |
分析 在电解水实验中,可观察到的现象有:正极的气体体积少,能使带火星的木条复燃,负极的气体体积多,能燃烧,而且体积多的是少的二倍.根据以上现象可推出正极产生的气体是氧气,负极产生的气体是氢气,还能进一步推出水由氢元素和氧元素组成,利用这些相关的知识解题.
解答 解:A、水通电分解生成氢气和氧气,说明水是由氢元素和氧元素组成的.故正确;
B、此实验为了增强水的导电性,常常往水中加入稀硫酸,故正确;
C、水通电分解生成氢气和氧气,水电解的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,故正确;
D、电解水正极是氧气,负极是氢气,a是氢气,b是氧气,体积比是2:1,质量比是1:8,若a试管气体为10g,则b试管气体为80g,故错误.
故选:D.
点评 电解水实验的重要现象:与负极相连的试管产生氢气,与电源正极相连的试管产生的为氧气,两种气体体积比为2:1.结论是水是由氢元素和氧元素组成的.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
18.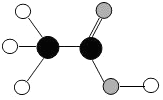 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,
代表一个碳原子, 代表一个氢原子,
代表一个氢原子, 代表一个氧原子,下列说法不正确的是( )
代表一个氧原子,下列说法不正确的是( )
 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,
代表一个碳原子, 代表一个氢原子,
代表一个氢原子, 代表一个氧原子,下列说法不正确的是( )
代表一个氧原子,下列说法不正确的是( )| A. | 乙酸的化学式CH3COOH | |
| B. | 乙酸的相对分子质量为60 | |
| C. | 乙酸中碳元素的质量分数为60% | |
| D. | 乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:1 |
18. 日本曾向美国借了331公斤武器级钚,至今赖着不还,钚除用于核电外,还是制造核武器的主要原料,现在日本已经是世界第六大钚拥有国,钚元素的相关信息如图,下列说法不正确的是( )
日本曾向美国借了331公斤武器级钚,至今赖着不还,钚除用于核电外,还是制造核武器的主要原料,现在日本已经是世界第六大钚拥有国,钚元素的相关信息如图,下列说法不正确的是( )
 日本曾向美国借了331公斤武器级钚,至今赖着不还,钚除用于核电外,还是制造核武器的主要原料,现在日本已经是世界第六大钚拥有国,钚元素的相关信息如图,下列说法不正确的是( )
日本曾向美国借了331公斤武器级钚,至今赖着不还,钚除用于核电外,还是制造核武器的主要原料,现在日本已经是世界第六大钚拥有国,钚元素的相关信息如图,下列说法不正确的是( )| A. | 钚是金属元素 | B. | 一个钚原子的质量为244g | ||
| C. | 钚的原子序数是94 | D. | 钚元素的原子核外有94个电子 |
15.写出化学用语:铁离子Fe3+ 亚铁离子Fe2+ 硝酸根离子NO3- 2个碳酸根离子2CO32-.
2个氢离子2H+;3个硫离子3S2-;4个氢氧根离子4OH-;+1价铜的氧化物Cu2O;
2个氢离子2H+;3个硫离子3S2-;4个氢氧根离子4OH-;+1价铜的氧化物Cu2O;
| 化学符号 | 6Mg | 3N2 |  | Zn2+ |
| 表示意义 | 六个镁原子 | 三个氮分子 | 核内有11个质子 | 一个锌离子 |
19.现有氢气、甲烷、二氧化碳三种气体,如果用最简单的方法将它们鉴别出来,除一盒火柴外,你还至少需要下列哪种试剂( )
| A. | 澄清石灰水 | B. | 蒸馏水 | C. | 酚酞试液 | D. | 浓硫酸 |


 向20克黄铜(由锌、铜形成的合金)样品加入稀盐酸充分反应,所加稀盐酸与生成气体的质量关系如图所示.求:黄铜样品中含铜的质量.
向20克黄铜(由锌、铜形成的合金)样品加入稀盐酸充分反应,所加稀盐酸与生成气体的质量关系如图所示.求:黄铜样品中含铜的质量.