题目内容
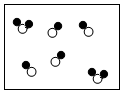
2.实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答:
【探究实验一】酸能否与可溶性碱发生化学反应
甲同学进行了实验一,能观察到的明显现象是溶液由红色变成了无色,同时测定反应后溶液的pH=2,说明酸能与可溶性碱发生化学反应.
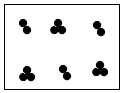
【探究实验二】酸能否与难溶性碱发生化学反应
乙同学进行了实验二,当滴入几滴稀盐酸后,发现试管②中无明显变化,于是得出“酸不能与难溶性碱反应”的结论.
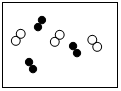
丙同学对此产生质疑,并利用实验后的物质继续探究:
【分析】丙同学测定试管②中上层清液的酸碱度,读出pH=12,说明上层清液中的溶质是氯化钠、硫酸钠、氢氧化钠.
【解释】丙同学由此认为乙同学的结论不正确,原因是加入的盐酸太少.
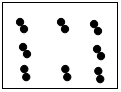
【验证】丙同学利用上述实验后的废液继续实验,将试管②中物质全部倒入一大烧杯中,静置,再将实验探究一所得溶液逐滴加入,能说明酸与难溶性碱发生化学反应的现象是蓝色沉淀慢慢消失.
【拓展】实验探究一、二中,均涉及到的反应的化学方程式是NaOH+HCl=NaCl+H2O.
丙同学将实验一所得溶液缓慢滴加的过程中,除上述现象外,大烧杯中还可观察到的现象是溶液由无色变成红色,然后由红色慢慢又变成无色.
分析 【探究实验一】根据酸碱指示剂的变色情况来分析;
【探究实验二】
【分析】根据溶液的pH来分析;
【解释】根据滴加的盐酸太少来分析;
【验证】根据实验探究一中所得溶液中含有盐酸来分析;
【拓展】根据两个实验中发生的化学反应以及探究二中的溶液显碱性来分析.
解答 解:【探究实验一】氢氧化钠溶液显碱性,能使无色的酚酞试液变红色,向烧杯中滴加稀盐酸,盐酸与氢氧化钠发生中和反应生成氯化钠和水,会观察到溶液的颜色由红色变成了无色;故填:溶液由红色变成了无色;
【探究实验二】
【分析】氢氧化钠与硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠;若测得试管②清液的pH=12,说明溶液显碱性,存在氢氧化钠,向试管②中滴加的几滴盐酸与氢氧化钠发生了中和反应,还没有来得及与氢氧化铜沉淀反应,所以没有观察到难溶性的氢氧化铜溶解,所以试管②中存在的溶质是氯化钠、硫酸钠、氢氧化钠;故填:氯化钠、硫酸钠、氢氧化钠;
【解释】试管②中的溶液中存在氢氧化钠,加入的盐酸太少,只与氢氧化钠发生了反应,没有与氢氧化铜反应,所以乙同学的结论不正确;故填:加入的盐酸太少;
【验证】探究一所得溶液显酸性,存在着HCl,将试管②中物质全部倒入一大烧杯中,静置,再将实验探究一所得溶液逐滴加入,盐酸与氢氧化钠反应生成氯化钠和水,盐酸与氢氧化铜反应生成氯化铜和水,会观察到蓝色沉淀慢慢消失,这说明酸与难溶性碱发生化学反应;故填:蓝色沉淀慢慢消失;
【拓展】两个实验中均发生了盐酸与氢氧化钠反应生成氯化钠和水这一反应;故填:NaOH+HCl=NaCl+H2O;
因为探究二中的溶液pH=12,显碱性,随着探究一中酸性溶液的加入,溶液慢慢变成中性,滴加过量后,溶液显酸性,因此将实验一所得溶液缓慢滴加的过程中,会观察到溶液由无色变成红色,然后由红色慢慢又变成无色;故填:溶液由无色变成红色,然后由红色慢慢又变成无色.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 五•一期间某同学从华蓥山上采集到一种石灰石,为了测定石灰石中CaCO3的含量.该同学取40克石灰石样品进行煅烧实验(所含杂质在煅烧过程中不发生变化,已知CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ ),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
五•一期间某同学从华蓥山上采集到一种石灰石,为了测定石灰石中CaCO3的含量.该同学取40克石灰石样品进行煅烧实验(所含杂质在煅烧过程中不发生变化,已知CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ ),测得反应后固体的质量(m)与反应时间(t)的关系如下表:| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 40 | 37.5 | 35 | 32.5 | 31 | 29 | 29 |
(1)从表中数据分析,加热到t5时间时CaCO3已经完全分解;
(2)当石灰石完全反应后,生成CO2的质量为11g;
(3)40克该石灰石中CaCO3的质量25g;
(4)请在如图坐标图中,绘出煅烧时生成气体的质量(m)随时间(t)变化的曲线.
| A. | 牡丹花做成花环 | B. | 柚子运到北京 | ||
| C. | 牛角雕成工艺品 | D. | 高粱发酵做成砸酒 |
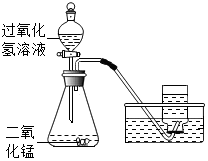 如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如表:
如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如表:| 气体发生装置内物质的总质量 | |
| 反应前 | 36.4g |
| 反应后 | 30.0g |
(2)反应生成氧气的质量为6.4g.
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程.
 下面关于水电解实验的叙述不正确的是( )
下面关于水电解实验的叙述不正确的是( )| A. | 实验说明水是由氢、氧两种元素组成的 | |
| B. | 此实验为了增强水的导电性,常常往水中加入稀硫酸 | |
| C. | 水电解的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| D. | 若a试管气体为10g,则b试管气体为5g |
| A. | 液氧用于火箭发射 | B. | 盐酸除铁锈 | ||
| C. | 钛合金制人造骨 | D. | 熟石灰用于改良酸性土壤 |
| A. | 钙是人体中的微量元素 | |
| B. | 鸡蛋含有丰富的蛋白质 | |
| C. | 淀粉不属于糖类,但可为人体提供能量 | |
| D. | 油脂是重要的营养物质,可大量摄入油脂 |