题目内容
19.某课外小组的同学以“铝、锌、铜的化学性质”为课题,进行科学探究活动,请根据己学知识完成下列探究问题.【提出问题】铝、锌、铜的金属活动性顺序是怎样的?
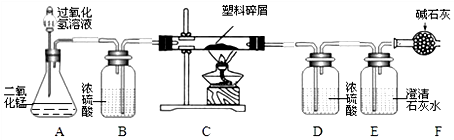
【制定计划】甲同学设计的实验如图所示,他们在实验中都进行了规范的操作和细致的观察.

【收集证据】你认为实验初①中没有观察到明显现象的原因是(1)铝片表面有氧化膜;实验②中应观察到的现象是(2)锌片表面产生气泡;
【解释与结论】乙同学认为甲同学的实验设计有错误,其理由是(3)没有除去金属表面的氧化膜,稀硫酸的浓度不同;
【反思与评价】反思后甲同学对自己的实验进行了改正,其作法是(4)打磨金属片,把稀硫酸改为浓度相同;由此证明了三者的金属活动性顺序是(5)铝>锌>铜.
【表达与交流】我国的金属矿物资源储量有限,且不可再生.请你提出一条保护金属资源的有效措施(6)合理开发金属资源.
分析 铝比锌活泼,锌比铜活泼;
一些金属比较活泼,通常情况下能和空气中的氧气反应生成氧化物保护膜;
合理开发金属资源,防止金属生锈,回收利用废旧金属,寻找金属替代品等,都可以得到保护金属资源的目的.
解答 解:【收集证据】
(1)实验初①中没有观察到明显现象的原因是铝片表面有氧化膜,先和稀硫酸反应生成盐和水;
(2)实验②中锌和稀硫酸反应生成硫酸锌和氢气,应观察到的现象是锌片表面产生气泡.
故填:铝片表面有氧化膜;锌片表面产生气泡.
【解释与结论】
(3)乙同学认为甲同学的实验设计有错误,其理由是:没有除去金属表面的氧化膜,稀硫酸的浓度不同,无法比较铝和锌的活泼性.
故填:没有除去金属表面的氧化膜,稀硫酸的浓度不同.
【反思与评价】
(4)反思后甲同学对自己的实验进行了改正,其作法是:打磨金属片,把稀硫酸改为浓度相同;
(5)实验过程中,观察到铝片表面产生气泡速率比锌片快,铜片表面无明显现象,说明铝比锌活泼,锌比铜活泼,由此证明了三者的金属活动性顺序是铝>锌>铜.
故填:打磨金属片,把稀硫酸改为浓度相同;铝>锌>铜.
【表达与交流】
合理开发金属资源,防止金属生锈,回收利用废旧金属,寻找金属替代品等,都可以得到保护金属资源的目的.
故填:合理开发金属资源.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
8.下列实验现象描述正确的是( )
| A. | 将氢氧化镁与酚酞溶液混合,观察酚酞溶液由无色变为红色 | |
| B. | 铜丝放入硝酸银溶液中:紫红色固体表面覆盖一层银白色固体,溶液由无色变为蓝色 | |
| C. | 将氧化铁中加入足量的稀硫酸,红棕色固体消失,溶液由无色变为黄色,放热 | |
| D. | 打开浓盐酸的瓶子时,瓶口处出现白烟 |
9.如图所示,依据A、B、C三种固体物质的溶解度曲线,判断下列说法不合理的是( )

| A. | 20℃时,A和C物质的溶解度相同 | |
| B. | 50℃时,50g水中最多溶解B物质的质量一定小于25g | |
| C. | A、B、C三种物质的溶液,都可以用蒸发溶剂的方法得到溶质固体 | |
| D. | 50℃时,A、B、C三种物质的饱和溶液各100g,分别降温到20℃,最后所得溶液的质量关系是A>C>B |
4.A、B、C三种固体物质的溶解度曲线如图所示,下列说法不正确的是( )


| A. | 10℃时,将30 g A物质放入50 g水中充分搅拌后所得溶液的质量为80 g | |
| B. | 将30℃时,A、B、C三种物质的饱和溶液降温到10℃,C的溶质质量分数保持不变 | |
| C. | 升高温度可以使C的不饱和溶液转变成饱和溶液 | |
| D. | 采用冷却热饱和溶液的方法可以从A、B的混合物中分离A物质 |
9.小明在协助老师清理实验室时,发现有一瓶碳酸钠和氢氧化钠组成的混合液,他想测定该溶液中碳酸钠的质量分数,为此设计并进行了如下实验:取该混合液50g,向其中逐滴加入稀盐酸,当加入稀盐酸的质量为20g、40g、60g时,生成气体的质量见下表(气体的溶解度忽略不计).则:
(1)m的数值是4.4.
(2)此混合溶液中碳酸钠的溶质质量分数是多少?
| 稀盐酸的质量/g | 20g | 40g | 60g |
| 生成气体的质量/g | 2.2 | m | 5.5 |
(2)此混合溶液中碳酸钠的溶质质量分数是多少?