题目内容
19.现欲通过实验确定一固体混合物A的成分,已知其中可能含有Na2CO3、NaCl、CuO、Cu(OH)2四种物质中的两种或多种.按如图所示进行实验,出现的现象如图中所述.(假设过程中所有发生的反应都恰好完全反应).
试根据以上实验过程和现象填写以下空白:
(1)气体B的化学式为CO2,固体G的颜色为红色.
(2)混合物A中,一定存在的物质是(写化学式)Na2CO3、CuO.
(3)滤液F中,一定大量存在的阴离子是(写离子符号)NO3-.
(4)写出实验过程③中所发生的一个化学反应的方式:CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2.
分析 根据已有的知识进行分析,固体混合物A加盐酸反应生成的气体B能使澄清的石灰水变浑浊,故B是二氧化碳,说明A中含有碳酸钠;由于得到的是溶液,故固体全部溶解,说明A中不含有铜;溶液C加硝酸银,得到白色沉淀,故C中含有氯化钠,可能是碳酸钠和盐酸反应生产的氯化钠,也可能是原来就有的氯化钠;滤液D加入铁粉充分反应生成滤液F和固体G,说明D中含有铜离子,故A中一定含有氧化铜,而D中含有氯化铜与硝酸银反应生成的硝酸铜,据此解答.
解答 解:固体混合物A加盐酸反应生成的气体B能使澄清的石灰水变浑浊,故B是二氧化碳,说明A中含有碳酸钠;由于得到的是溶液,故固体全部溶解,说明A中不含有铜;溶液C加硝酸银,得到白色沉淀,故C中含有氯化钠,可能是碳酸钠和盐酸反应生产的氯化钠,也可能是原来就有的氯化钠;滤液D加入铁粉充分反应生成滤液F和固体G,说明D中含有铜离子,故A中一定含有氧化铜,而D中含有氯化铜与硝酸银反应生成的硝酸铜,带入框图,推断合理;
(1)根据分析,B是二氧化碳,固体G为铜,其颜色为红色.故填:CO2;红;
(2)根据分析,A中一定含有碳酸钠和氧化铜,故填:Na2CO3、CuO;
(3)根据分析,因为③加入硝酸银溶液,则滤液F中,一定大量存在的阴离子是NO3-.
(5)实验过程③中所发生的一个化学反应的化学方程式为:CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2或NaCl+AgNO3=NaNO3+AgCl↓;
故答案为:
(1)CO2;红色;(2)Na2CO3;(3)NO3-;(4)CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2 (或NaCl+AgNO3=NaNO3+AgCl↓)
点评 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.本题考查了常见物质成分的推断,完成此题可以依据题干提供的信息结合物质的性质进行.

 阅读快车系列答案
阅读快车系列答案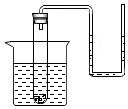 把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )
把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )| A. | 减少、左高右低 | B. | 增加、左高右低 | C. | 减少、左低右高 | D. | 增加、左低右高 |

(1)“信使”号发回的最新照片上显示,水星上确有固态水存在.如图微粒模型示意图中能表示构成水的微粒的是B(填序号).
(2)水星上含有丰富的二氧化碳和镁资源.科学家设想,镁可作为未来水星上的燃料,因为镁能在二氧化碳中燃烧放出大量的热,同时生成氧化镁和碳.该反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(3)上述反应属于置换反应类型.
(4)水星北极的土壤呈弱碱性.如果水星具备作物生长的条件,下表所列作物较适宜在水星北极种植的有芦笋、萝卜.
| 作物名称 | 芦笋 | 草莓 | 萝卜 | 马铃薯 |
| 适宜生长的pH | 6.5~7.8 | 5.5~6.5 | 7~8 | 5.6~6 |
| A. | 煤气中毒通常是指一氧化碳中毒 | |
| B. | 分子、原子、离子都是构成物质的微粒 | |
| C. | 烧碱长时间露置于空气中其成分会发生变化 | |
| D. | 生成单质和化合物的反应一定是置换反应 |
(1)一种非金属单质O2(或H2或O3或C);
(2)最简单的有机物CH4;
(3)一种碱NaOH;
(4)俗称纯碱的盐Na2CO3.
| A. | NH4+、Cu2+、SO42-、NO3- | B. | K+、Ba2+、Cl-、SO32- | ||
| C. | K+、MnO4-、NH4+、CH2COO- | D. | Na+、K+、HCO3-、NO3- |
| A. |  加热液体 | B. |  点燃酒精灯 | C. |  添加酒精 | D. |  熄灭酒精灯 |
| 化学符号 | 4N | |||
| 表示意义 | 正一价的氢 | 两个氧分子 | 硫酸根离子 |
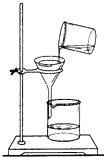 小亮同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤.请回答下列问题.
小亮同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤.请回答下列问题.