题目内容
7.如图所示是实验室常见的制取气体的装置: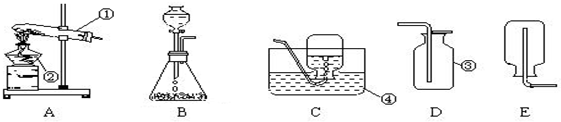
(1)写出仪器名称:①试管②酒精灯③集气瓶④水槽.
(2)实验室采用高锰酸钾制取氧气时,应选择的发生装置是A(填序号,下同),试管口还要塞一团棉花,目的是防止高锰酸钾粉末进入导管,反应的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,此反应属于分解反应.(填“化合”或“分解”).
(3)实验室采用过氧化氢溶液制取氧气时,应选择的发生装置是B,反应的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,它与采用装置A制取氧气时比较,主要优点是不用加热,节约能源(任答一条).
(4)收集氧气可以选择装置C,你选择它的理由是氧气不易溶于水.若用排水法收集氧气时,当观察到气泡连续均匀冒出时才开始收集,否则收集的氧气不纯.某同学收集完毕,先停止加热再将导管移出水面,你预测这种操作可能会引起的后果是水槽中水倒流,炸裂试管,如果选用D收集氧气,验满的方法是将带火星的木条放在集气瓶口,木条复燃,证明集满.
(5)在做铁丝在氧气中燃烧的实验时,要预先在集气瓶底铺一层细沙或留有少量的水,其目的是防止高温的生成物炸裂瓶底.
(6)实验室常用加热无水醋酸钠和碱石灰固体的方法制取甲烷气体,已知甲烷难溶于水,比空气的密度小.则制备甲烷气体需要发生装置是A(填序号,下同),要想收集更纯净的甲烷气体,最好选用的收集装置是C.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的生成锰酸钾、二氧化锰和氧气进行分析;
(3)根据实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
(4)根据氧气密度比空气大,不易溶于水,收集方法有:向上排空气法和排水法,以及收集氧气的正确时刻,制取氧气的正确操作方法,氧气的助燃性进行分析;
(5)根据玻璃是热的玻璃导体进行分析;
(6)根据实验室制取甲烷的反应物是固体,反应条件是加热,甲烷难溶于水,比空气的密度小进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是试管,②是酒精灯,③是集气瓶,④是水槽;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选择的发生装置是A,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的生成锰酸钾、二氧化锰和氧气,文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,该反应满足分解反应一变多的条件,属于分解反应;
(3)实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,所以应选择的发生装置是B,过氧化氢在二氧化锰的催化作用下生成水和氧气,文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,与采用装置A制取氧气时比较,主要优点是:不用加热,节约能源;
(4)氧气密度比空气大,不易溶于水,收集方法有:向上排空气法和排水法,若用排水法收集氧气时,当观察到气泡连续均匀冒出时才开始收集,否则收集的氧气不纯,收集完毕,先停止加热再将导管移出水面,预测这种操作可能会引起的后果是:水槽中水倒流,炸裂试管,氧气的助燃性,所以验满的方法是:将带火星的木条放在集气瓶口,木条复燃,证明集满;
(5)玻璃是热的玻璃导体,所以在做铁丝在氧气中燃烧的实验时,要预先在集气瓶底铺一层细沙或留有少量的水,其目的是:防止高温的生成物炸裂瓶底;
(6)实验室制取甲烷的反应物是固体,反应条件是加热,甲烷难溶于水,比空气的密度小,所以制备甲烷气体需要发生装置是A,要想收集更纯净的甲烷气体,最好选用的收集装置是C.
故答案为:(1)试管,酒精灯,集气瓶,水槽;
(2)A,防止高锰酸钾粉末进入导管,高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,分解;
(3)B,过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,不用加热,节约能源;
(4)C,氧气不易溶于水,连续均匀冒出,水槽中水倒流,炸裂试管,将带火星的木条放在集气瓶口,木条复燃,证明集满;
(5)防止高温的生成物炸裂瓶底;
(6)A,C.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 习题精选系列答案
习题精选系列答案①试管 ②集气瓶 ③量筒 ④烧杯 ⑤石棉网.
| A. | ①⑤ | B. | ①② | C. | ①③④ | D. | ②③④ |
| A. | 氧气 | B. | 铁丝 | C. | 二氧化碳 | D. | 水 |
 从碳酸钠、氢氧化钠、稀盐酸、氯化钡、氯化钠几种溶液中取出其中的两种混合,回答下列问题:
从碳酸钠、氢氧化钠、稀盐酸、氯化钡、氯化钠几种溶液中取出其中的两种混合,回答下列问题: 按照下列要求,完成计算.
按照下列要求,完成计算.